Enfermedad de Crohn
Enfermedad de Crohn
M.J. Martínez Gómez, J.F. Viada Bris.
Sección de Gastroenterología. Hospital Infantil Universitario Niño Jesús. Madrid.
Adolescere 2015; III (2): 54-62
Resumen
|
La enfermedad inflamatoria intestinal (EII) engloba a un grupo de entidades que se caracterizan por la inflamación crónica en diferentes localizaciones del tubo digestivo. En el caso de la Enfermedad de Crohn esta inflamación puede afectar a cualquier parte del tracto digestivo desde la boca hasta el ano de forma segmentaria y transmural. La sintomatología y gravedad estará influenciada por la extensión, localización, grado de actividad inflamatoria y manifestaciones extraintestinales asociadas a la enfermedad. Además, en los pacientes en edad pediátrica deberemos asegurar un estado nutricional y crecimiento adecuados, junto con un desarrollo puberal completo y al igual que en todas las enfermedades crónicas en la infancia cuidar los aspectos psicosociales que estas conllevan en la infancia y adolescencia. Por ello el tratamiento, además de asegurar el control de los síntomas propios de la enfermedad, deberá orientarse para asegurar la maduración de un organismo en crecimiento. Palabras clave: Enfermedad inflamatoria intestinal; Enfermedad de Crohn; Adolescencia. |
Abstract
|
Inflammatory bowel disease (IBD) encompasses a group of entities that are characterized by chronic inflammation of different locations in the gastrointestinal tract. In the case of Crohn´s disease, this inflammation can affect any part of the gastrointestinal tract, from the mouth to the anus, in a segmental and transmural manner. The symptoms and severity will be influenced by the extent, location, degree of inflammatory activity and extra-intestinal manifestations associated with the disease. Moreover, in pediatric patients adequate nutritional status and growth must be ensured, along with a full pubertal development and, as in all chronic diseases during childhood and adolescence, care for psychosocial aspects should be provided. Therefore, the treatment must securely control the symptoms of the disease, but also strive to ensure the development of a growing organism. Key words: Inflammatory bowel disease; Crohn’s disease; Adolescence. |
Caso clínico
Enfermedad actual: Varón de 13 años y 4 meses ingresado en Planta de Hospitalización de Pediatría y valorado por Gastroenterología por cuadro de varios meses de evolución de dolor abdominal localizado en fosa iliaca derecha. Refiere que el dolor es continuo y no irradiado. En su inicio, aparecía con una frecuencia de tres o cuatro veces por semana aumentando su frecuencia e intensidad hasta el momento de la primera consulta, en el que se presenta de forma diaria. No presenta predominio horario. No lo relacionan con ningún alimento ni está influenciado por la ingesta. Tampoco lo relaciona con ningún evento estresante.
Asocia astenia, hiporexia moderada y pérdida de peso de hasta 6 Kg desde el inicio del cuadro. Le despierta ocasionalmente por la noche e interfiere parcialmente con sus actividades de la vida diaria. No ha presentado vómitos ni sensación nauseosa. Tampoco ha presentado pirosis, ascenso de alimentos a la boca ni otra sintomatología del tracto digestivo superior.
Seis semanas antes de consultar presenta dolor con la defecación, tenesmo y hematoquecia intermitente. Realiza de tres a cuatro deposiciones al día de consistencia blanda (Tipo 5-6 de la escala de Bristol). Con la aparición de la hematoquecia acudió a su pediatra objetivándose dos fisuras anales que fueron tratadas con corticoide tópico sin conseguir el control de la sintomatología. No cuadros previos de fiebre de origen desconocida. No artralgias, ni lesiones cutáneas ni aftas orales.
Ante el aumento del dolor e inicio de fiebre acude al Servicio de Urgencias, donde se evidencia en la exploración física un absceso perianal. Dada la historia referida por el paciente y ante los hallazgos de la exploración física se decidió ingreso para completar estudio ante la sospecha de EII.
Antecedentes personales: Embarazo controlado cursó con normalidad. Parto a término, eutócico. Peso de recién nacido: 3230 g. Periodo neonatal: normal. Pruebas metabólicas y screening auditivo normales. Meconiorrexis en primeras 24 horas. Alimentación con lactancia mixta desde el nacimiento. Diversificación alimentaria reglada por su pediatra sin incidencias. No vomitador ni regurgitador en periodo de lactante. Desarrollo psicomotor: normal. Desarrollo ponderoestatural: ascendente. No alergias conocidas. Vacunas según calendario de la Comunidad Autónoma de Madrid. No refieren enfermedades de interés previas para el proceso actual.
Antecedentes familiares: No refieren existencia de enfermedades de origen autoinmune ni digestivas.
Exploración física: Peso: 40 Kg (P25). Talla: 155 cm (P50) IMC: 16,6 Buen estado general. Regular estado de nutrición con masas musculares blandas y escaso panículo adiposo. Palidez mucocutánea. Auscultación cardiaca: rítmica, soplo sistólico I-II/VI en borde esternal izquierdo. Auscultación pulmonar: normal. Abdomen blando y depresible. Dolor a la palpación superficial y profunda en fosa iliaca derecha. No se palpan masas ni visceromegalias. Exploración anal: eritema perianal intenso. No presencia de fisuras. Tacto rectal: doloroso. Abombamiento de pared izquierda del canal anal. ORL: normal. Genitales externos masculinos normales. Testes en bolsa. Estadío de Tanner 2-3.
Pruebas complementarias: Analítica al ingreso
Hemograma: Leucocitos 16,57×1000/uL (neutrófilos 71,4%, cayados 4%), Hb:11,8 g/dl, VCM: 70 fl, Plaquetas:468.000×1000/uL. VSG: 58 mm. T. protrombina: 85%. Fósforo:4,9 mg/dl, Calcio:9,4 mg/dl, F. alacalina:66 U/L. Fe sérico 33 ug/dl. Ferritina 96 ng/ml. Proteínas totales: 6,1 mg/dl. Albúmina: 2,8 mg/dl. PCR: 11,5 mg/dl. Orosomucoide: 264 mg/dl. Calprotectina fecal:> 600 ug/g
Resonancia magnética pélvica: trayecto fistuloso interesfinteriano con inicio en segmento medio de conducto anal, con signos de actividad pero sin cambios inflamatorios circundantes ni imagen de absceso actual.
Endoscopia digestiva alta: Esofagitis grado I, pangastritis con úlceras antrales duodenitis aftoide.
Colonoscopia: Pancolitis severa con múltiples úlceras aftoides a lo largo del trayecto y afectación ileal compatible con Enfermedad de Crohn activa.
Anatomía patológica: Esófago: esofagitis grado I. Fundus y antro gástrico: Gastritis crónica moderada con marcada actividad inflamatoria a expensas de linfocitos y polimorfonucleares y ulceración inespecífica. No se observa H.pylori. Duodeno: patrón vellositario conservado sin lesiones relevantes. Ileon: inflamación inespecífica. Colon: mucosa con arquitectura distorsionada, incremento de población linfoplamocitaria en lámina propia, y polimorfonucleares que permean el epitelio de las criptas. Granulomas epiteliodes no necrotizantes en todas las muestras. Conclusión: Cambios compatibles con Enfermedad inflamatoria intestinal idiopática (Enfermedad de Crohn).
Tratamiento
En este paciente se empleó como tratamiento la nutrición por vía oral exclusiva con dieta polimérica isocalórica suplementada en TGF-beta, con un volumen total en 24 horas de 2000 ml, repartidos en 6-7 tomas a lo largo del día, durante 8 semanas. Durante los primeros 15 días recibió metronidazol oral lo que permitió el cierre del trayecto fistuloso. Se inició asimismo tratamiento con azatioprina a dosis de 2,5 mg/Kg. Se planteó la posibilidad de comenzar el tratamiento con un fármaco biológico, dada la afectación perianal, pero la buena respuesta conseguida con tratamiento nutricional y azatioprina hizo innecesario esta pauta. Se indicaron suplementos de sulfato ferroso, calcio y vitamina D3.
Evolución
La evolución fue muy satisfactoria desde el inicio, desapareciendo la sintomatología en 2 semanas, normalizando los parámetros inflamatorios, y tolerando a partir de las 6 semanas de tratamiento, la reintroducción progresiva de alimentación normal. En la última revisión 4 meses después del debut de la enfermedad, el peso es 46 Kg y la talla 157 cm. Sigue tomando como suplemento nutricional dieta polimérica.
Enfermedad de Crohn
Definición
La enfermedad inflamatoria intestinal (EII) engloba a un grupo de entidades que se caracterizan por la inflamación crónica en diferentes localizaciones del tubo digestivo. Bajo este término se engloban la enfermedad de Crohn (EC), la colitis ulcerosa (CU) y la enfermedad inflamatoria no clasificada (EIInC). Su curso clínico se caracteriza por alternar periodos de inactividad o remisión con periodos de actividad clínica denominados brotes o recidivas.
En la enfermedad de Crohn, la inflamación puede afectar a todo el tubo digestivo desde la boca hasta el ano de forma segmentaria.
En la enfermedad de Crohn, la inflamación puede afectar a todo el tubo digestivo desde la boca hasta el ano de forma segmentaria, siendo su característica histológica la afectación transmural de la mucosa y la presencia de granulomas no caseificantes.
Epidemiologia
En la actualidad se ha demostrado un aumento de la incidencia de la EII pediátrica a nivel mundial sobre todo a expensas de la EC. El registro pediátrico español refiere un aumento de incidencia en los últimos veinticinco años de 2,51 casos por 100.000 habitantes y año, en pacientes menores de 18 años hasta el año 2010, siendo 1,7 casos por 100.000 EC. La EC es más frecuente en varones (59%) existiendo un pico de incidencia en la infancia tardía y adolescencia entre los 12 y 14 años.
Etiopatogenia
La EII es una enfermedad compleja y poligénica en cuya patogenia se implican distintos factores genéticos y ambientales. Se considera que existe una base genética que condiciona una respuesta inmune anómala a determinadas variaciones en la microflora bacteriana.
La posibilidad de desarrollar EII cuando uno de los padres está afectado es de 9,2% para la EC. Cuando padre y madre padecen EII el riesgo de padecerla los hijos aumenta hasta 30%. Asimismo la concordancia en padecer la enfermedad en gemelos apoya la base genética de la misma.
Distintos genes se han asociado con EII. El gen que codifica NOD2, situado en cromosoma 16, renombrado como CARD15 a partir de la publicación del genoma humano, se ha asociado con EC de inicio temprano y con EC estenosante. La explicación a este hecho está en la función de CARD15 en el reconocimiento bacteriano, la apoptosis y la señalización inflamatoria.
Otros factores genéticos sin influir en la susceptibilidad pueden sin embargo condicionar el curso de la misma como la presencia de HLA DR2 asociado con colitis ulcerosa en japoneses, el DR3-DQ2 con pancolitis ulcerosa, HLA-DRB*0103*con presencia de manifestaciones extraintestinales y con la necesidad de cirugía en la EC.
Existe por tanto una disregulación genéticamente determinada de la respuesta inmune frente a la flora bacteriana que da lugar a activación de linfocitos TCD4 y que produce una Inflamación intestinal incontrolada que se autoperpetua por aumento de mediadores proinflamatorios La respuesta inmune es diferente en ambas entidades estando en el caso de EC mediada por Th1 y en la CU por anticuerpos
Distintos factores ambientales se ha relacionado con la EII, entre ellos la lactancia materna como protector para el desarrollo de la misma, el tipo de dieta, el tabaco y la apendicectomía previa (protectores para CU y de riesgo para EC).
Existe por tanto una disregulación genéticamente determinada de la respuesta inmune frente a la flora bacteriana que da lugar a activación de linfocitos TCD4 y que produce una Inflamación intestinal incontrolada.
Clínica
La forma de presentación más característica de la EC es el dolor abdominal, diarrea y pérdida de peso. Esta triada clásica sólo aparecerá en el 25% de los pacientes siendo más frecuente que los síntomas se presenten de forma larvada e insidiosa. El dolor suele localizarse en fosa iliaca derecha o en región periumbilical, pudiendo presentar además los pacientes epigastralgia o dispepsia en los casos en los que exista afectación del tracto digestivo superior.
La forma de presentación más característica de la EC es el dolor abdominal, diarrea y pérdida de peso. Esta triada clásica sólo aparecerá en el 25% de los pacientes.
Las manifestaciones clínicas de la enfermedad de Crohn pueden clasificarse en digestivas y extradigestivas. A estos síntomas en la edad pediátrica debemos añadir el retraso del crecimiento y el retraso puberal. Las manifestaciones clínicas intestinales de la EC son:
• Dolor abdominal recurrente.
• Diarrea: puede acompañarse de molestias abdominales previas a la defecación y urgencia rectal.
• Masa abdominal: en la exploración abdominal puede palparse una masa abdominal en fosa iliaca derecha. Si este hallazgo se acompaña de fiebre o febrícula de origen desconocido el diagnóstico de EC debe ser considerado.
• Enfermedad perianal/fístulas: en pediatría puede ser la forma de debut de la enfermedad entre el 15-25%.
• Anorexia y pérdida de peso.
• Anemia ferropénica refractaria a tratamiento.
En cuanto a las manifestaciones extradigestivas quedan recogidas en la tabla I.
Clasificación de la Enfermedad de Crohn
La clasificación de la enfermedad de Crohn tiene en cuenta la expresión fenotípica de la enfermedad. Su uso pretende establecer las herramientas terapéuticas adecuadas y establecer el pronóstico de la enfermedad. En la tabla II quedan recogidas la clasificación de Montreal (2006) y de París (2011).
Diagnóstico:
La EC puede presentarse de forma insidiosa y con sintomatología larvada y poco evidente, lo que puede provocar la demora diagnóstica. Es prioritario establecer el diagnóstico precoz teniendo en cuenta la idiosincrasia del paciente pediátrico. Su diagnóstico se basa en la combinación de datos clínicos, exploración física, exámenes de laboratorio y técnicas endoscópicas y de imagen. Para establecer el diagnóstico de certeza entre EC, CU y EIInC, los criterios de Oporto revisados por última vez en el año 2014, establecen la necesidad de realizar en todos los pacientes con sospecha de EII: endoscopia digestiva alta, endoscopia digestiva baja con ileoscopia, biopsias múltiples de todas las porciones exploradas y técnicas de imagen para el estudio del intestino delgado (preferentemente enteroRM o cápsula endoscópioca).
La anemia ferropénica es una constante en los casos de EII y puede preceder durante años al diagnóstico de EC. Aunque los datos analíticos son inespecíficos la existencia de reactantes de fase aguda elevados aún en ausencia de clínica digestiva es orientativa de EII.
Laboratorio: La anemia ferropénica es una constante en los casos de EII y puede preceder durante años al diagnóstico de EC. Aunque los datos analíticos son inespecíficos la existencia de reactantes de fase aguda elevados aún en ausencia de clínica digestiva es orientativa de EII: VSG, PCR, orosomucoide, fibrinogeno, ferritina. En brote agudo se puede encontrar además: leucocitosis, trombocitosis e hipoalbuminemia La ferritina es un reactante de fase aguda por lo que la anemia ferropénica no se acompaña de ferritina baja. La calprotectina fecal como proteína de degradación de polimorfonucleares es el marcador más sensible de inflamación intestinal y su elevación es discriminativa en el diagnóstico de brote agudo de la enfermedad. La determinación de p-ANCA (anticuerpo anticitoplasma perinuclear de los neutrófilos) y ASCA (anticuerpo anti- Sacharomyces cerevesiae) puede ser útil en caso de diagnóstico dudoso, p-ANCA es positivo en 50-60% de CU y 5-10% en EC, ASCA en 50-80% de EC y 10% de CU. Su negatividad no excluye la enfermedad.
Endoscopia: La endoscopia puede diferenciar la CU de la EC aproximadamente en el 80-90% de los casos. Las características endoscópicas de la Enfermedad de Crohn son:
• Úlceras (aftosas, lineales, serpinginosas)
• Mucosa de empedrado.
• Lesiones aisladas.
• Estenosis.
• Fístulas.
• Anomalías en la región oral y/o perianal.
• Distribución segmentaria.
En cuanto a la histología propia de la EC los hallazgos característicos son:
• Afectación submucosa (en biopsia con suficiente tejido submucoso) o transmural (pieza quirúrgica).
• Abcesos crípticos.
• Granulomas (no saceificantes).
• Cambios focales (en la biopsia).
• Distribución parcheada (en la biopsia).
Pruebas de imagen: En la actualidad el transito gastrointestinal baritado, ha sido sustituido por la entero resonancia magnética que aporta una excelente calidad de imagen en la localización de lesiones de intestino delgado y que tiene como ventaja la ausencia de radiación para el paciente. Precisa la colaboración del niño, que debe ingerir un alto volumen de líquido, lo que impide realizar la prueba bajo anestesia e imposibilita la realización en niños pequeños. En los casos en que la prueba no pueda realizarse o no se disponga de esta posibilidad diagnóstica en el centro, puede recurrirse a la práctica de capsuloendoscopia.
Pruebas de imagen: En la actualidad el transito gastrointestinal baritado, ha sido sustituido por la entero resonancia magnética que aporta una excelente calidad de imagen en la localización de lesiones de intestino delgado.
La resonancia magnética de la región pélvica es imprescindible en aquellos casos de Enfermedad de Crohn con afectación perianal o en aquellos en que exista sospecha de enfermedad fistulizante.
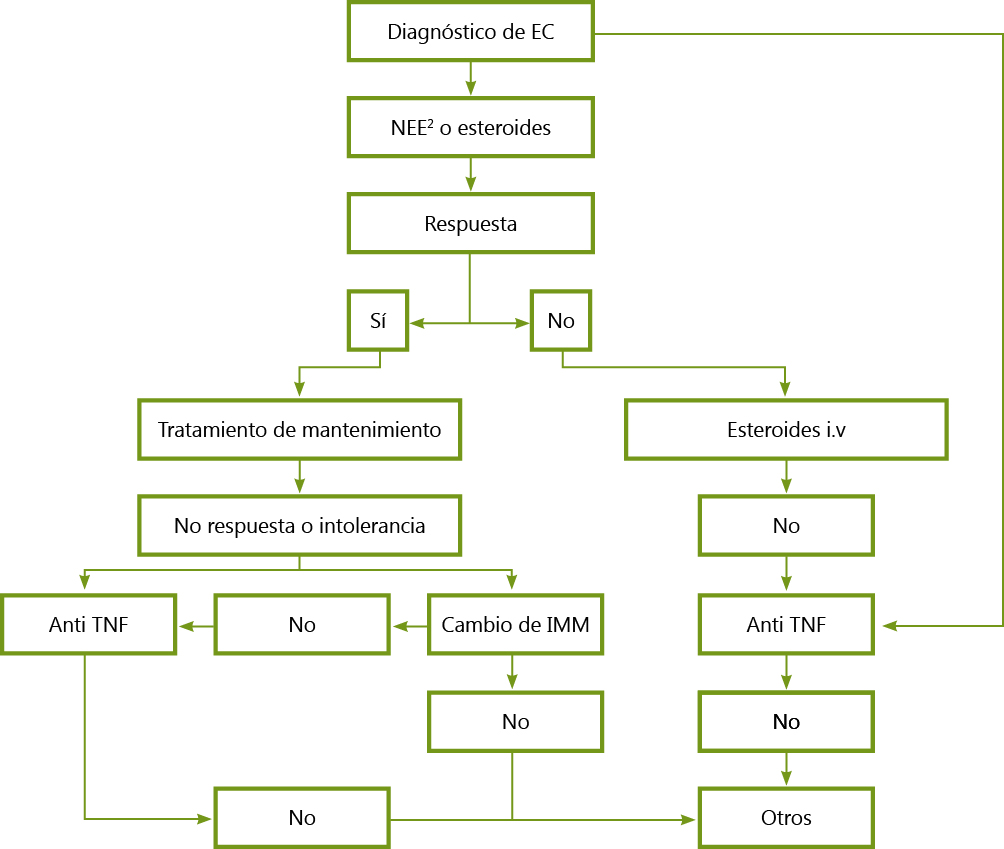
El algoritmo diagnóstico cuando exista sospecha de EII, queda reflejado en la Figura 1.
Tratamiento
La mayoría de los fármacos utilizados en la EII pediátrica, han sido adaptados a partir de la experiencia en adultos con la única modificación de su adecuación al peso del niño. Sin embargo es obligado dadas las características de la enfermedad en estas edades, con repercusión importante sobre el crecimiento y desarrollo, el abordaje de la misma atendiendo a los aspectos nutricionales. Conseguir la recuperación nutricional es uno de los objetivos prioritarios, pero no menos importante es el efecto terapéutico en sí mismo de la nutrición, no solamente por su impacto sobre el crecimiento, sino también porque gracias a su papel inmunomodulador da lugar a la curación de la mucosa y la remisión clínica.
La creación de equipos multidisciplinarios que atiendan a estos pacientes en el contexto de Unidades de cuidado integral de EII, es fundamental para el manejo clínico de los aspectos médicos, quirúrgicos, nutricionales y psicosociales que la enfermedad conlleva.
Aminosalicilatos: La sulfasalazina ha sido sustituida en los últimos años por compuestos derivados del 5-aminosalicilico (5ASA), debido a sus innumerables efectos secundarios. La mesalazina puede utilizarse como tratamiento inicial de la EII en brote leve a moderado. Los 5ASA están indicados en presencia de enfermedad cólíca, aunque existen preparaciones en gránulos con cubierta entérica que son eficaces en íleon distal. Su utilización en colitis ulcerosa a largo plazo puede prevenir la aparición de cáncer, pero su eficacia en el mantenimiento a largo plazo en EC es escasa.
Corticoides: Se puede utilizar prednisona o 6-metil prednisolona por via oral o intravenosa respectivamente o budesonida disponible en cápsulas y enemas para tratamiento local. Los corticoides son eficaces en inducir la remisión en EII en un porcentaje elevado de pacientes, pero los importantes efectos secundarios que conllevan los hace desaconsejables como terapia de mantenimiento.
Antibioticos: Los antibióticos pueden ser útiles en determinadas formas de EII, modulando la respuesta inmune a las bacterias intestinales causantes de la inflamación. En la EC perianal o fistulizante y en casos de reservoritis, estaría indicado utilizar metronidazol o ciprofloxacino.
Inmunomoduladores: La azatioprina y la 6-mercaptopurina son los inmunomoduladores más utilizados en el mantenimiento de la remisión tanto de EC como de CU. Los niveles terapéuticos se alcanzan entre 8-12 semanas de inicio de tratamiento. La instauración precoz de tratamiento con azatioprina se asocia con mejor evolución a largo plazo de la enfermedad con una tasa menor de recurrencia. En el momento actual se recomienda iniciar tratamiento con azatioprina en el primer brote de EC junto con terapia nutricional, manteniendo el inmunomodulador hasta al menos 2 años después del último episodio de actividad y al menos hasta después de finalizado el crecimiento. Cuando la azatioprina es mal tolerada puede recurrirse a inmunomoduladores de segunda línea: metrotexate, ciclosporina o tacrolimus o bien iniciar tratamiento con fármacos biológicos anti- TNF.
Anticuerpos anti factor de necrosis tumoral (Anti-TNF): En el momento actual tanto el infliximab (IFX) que es un anticuerpo monoclonal quimérico humano (75%) y murino (25%), como el adalimumab (ADA; 100% humano) tienen indicación para el tratamiento de la Enfermedad de Crohn pediátrica. La objetivación de que la respuesta es mejor en aquellos casos en que el tratamiento se instaura en los dos primeros años tras el debut clínico y en pacientes jóvenes ha conducido a invertir en algunos casos la estrategia terapéutica pudiendo indicarse como tratamiento inicial en: EC extensa, fistulizante o perianal y en aquellos casos que se acompañan de manifestaciones extradigestivas.
Tratamiento nutricional: La terapia nutricional cumple una doble función: por una parte de soporte nutricional, corrigiendo las deficiencias de micro y macronutrientes y aportando las proteínas y calorías necesarias para la recuperación del estado nutricional y por otra parte terapéutica. En la EC constituye una importante alternativa al tratamiento con corticoides. Diversos trabajos en EC pediátrica han demostrado que la terapia nutricional es tan eficaz como los corticoides para inducir la remisión, careciendo de los efectos adversos sobre el crecimiento de estos. Los mejores resultados de la nutrición enteral exclusiva se dan en pacientes de nuevo diagnóstico con afectación ileal, con peor respuesta en la EC gastroduodenal, perianal o las manifestaciones extradigestivas. La utilización de dieta polimérica modificada con adición de TGF-beta parece ser más eficaz que la dieta polimérica convencional en la disminución de los índices de actividad clínicos y de IL-1B, IL-8 e Interferon gamma en mucosa intestinal.
Cirugía: Los pacientes con EC pueden precisar cirugía a lo largo de su vida sobre todo para el tratamiento de fístulas y abcesos y en casos de cuadros obstructivos por estenosis fundamentalmente de ileon terminal. El tratamiento quirúrgico en este último caso mantiene la remisión durante periodos prolongados. El protocolo terapéutico en EC de nuevo diagnóstico se recoge a continuación
La terapia nutricional cumple una doble función: por una parte de soporte nutricional, corrigiendo las deficiencias de micro y macronutrientes y aportando las proteínas y calorías necesarias para la recuperación del estado nutricional y por otra parte terapéutica.
Tablas y figuras
Figura 1. Algoritmo terapéutico para la EC pediátrica, con exclusión de la enfermedad perianal
Tomado de: Enfermedad Inflamatoria Intestinal en Pediatría. Ergón. 2013.
Bibliografía
1. Beattie RM, Croft NM, Fell JM, Afzal NA, Heuschkel RB. Inflammatory bowel disease. Arch Dis Child, 2006;91:426-432.
2. Martín-de-Carpi J, Rodríguez A, Ramos E, Jiménez S, Martínez-Gómez MJ, Medina E; SPIRIT-IBD Working Group of Sociedad Española de Gastroenterología, Hepatología y Nutricion Pediátrica. Increasing incidence of pediatric inflammatory bowel disease in Spain (1996-2009): the SPIRIT Registry. Inflamm Bowel Dis. 2013;19(1):73-80.
3. IBD Working Group of the European Society for Paediatric Gastroenterology, Hepatology and Nutrition (ESPGHAN) Inflammatory Bowel Disease in Children and Adolescents: Recommendations for Diagnosis. The Porto Criteria. J Pediatr Gastroenterol Nutr, 2005; 41:1–7
4. IBD Working Group of the European Society for Paediatric Gastroenterology Hepatology and Nutrition. Inflammatory bowel disease in children and adolescents: recommendations for diagnosis—the Porto criteria. J Pediatr Gastroenterol Nutr 2014: 58:6:795-806.
5. Working Group of the North American Society for Pediatric Gastroenterology, Hepatology, and Nutrition and the Crohn’s and Colitis Foundation of America. Differentiating Ulcerative Colitis from Crohn Disease in Children and Young Adults. J Pediatr Gastroenterol Nutr 2007;44:653–674
6. SilverbergMS, Satsangi J, Ahmad T, Arnott ID, Bernstein CN, Brant SR et al. Toward and integrated clinical, molecular and serological classification of inflammatory bowel disease. Report of a working party of the 2005 Montreal World Congress of Gastroenterology.Can J Gastroenterol 2005;19(supl A):5-36
7. Dotson JL, Hyams JS, Markowitz J, et als. Extraintestinal manifestations of pediatric inflammatory bowel disease and their relation to disease type and severity. J Pediatr Gastroenterol Nutr. 2010; 51(2):140-145.
8. Vucelic B. Inflammatory bowel disease: Controversies in the use of diagnostic procedures. Dig Dis. 2009;27(3):269-77.
9. Hyams J, Crandall W, Kugathasan S, Griffiths A, Olson A, Johanns J, Liu G, Travers S, Heuschkel R, Markowitz J, Cohen S, Winter H, Veereman-Wauters G, Ferry G, Baldassano R; REACH Study Group. Induction and maintenance infliximab therapy for the treatment of moderate-to-severe Crohn’s disease in children. Gastroenterology. 2007; 132(3): 863-73.
10. Rosh JR, Lerer T, Markowitz J, Goli SR, Mamula P, Noe JD, Pfefferkorn MD, Kelleher KT, Griffiths AM, Kugathasan S, Keljo D, Oliva-Hemker M, Crandall W, Carvalho RS, Mack DR, Hyams JS. Retrospective Evaluation of the Safety and Effect of Adalimumab Therapy (RESEAT) in pediatric Crohn’s disease. Am J Gastroenterol. 2009; 104(12): 3042-9.
11. Medina E, Urruzuno P, Manzanares J. Tratamiento con nutrición enteral de la enfermedad de Crohn en el niño. Enf Inf Intest al día.2007:6:105-110.
12. Hartman C, Berkowitz D, Weiss B, Shaoul R, Levine A, Adiv OE, Shapira R, Fradkin A, Wilschanski M, Tamir A, Shamir R Nutritional supplementation with polymeric diet enriched with transforming growth factor-beta 2 for children with Crohn’s disease.Isr Med Assoc J. 2008;10(7):503-7.