Vacunas en la adolescencia
Vacunas en la adolescencia
F.A. Moraga-Llop.
Pediatra. Vicepresidente 1º de la Asociación Española de Vacunología. Miembro del Consejo Asesor de Vacunaciones del Departamento de Salud de la Generalitat de Cataluña. Asesor Externo del Comité Asesor de Vacunas de la Asociación Española de Pediatría.
Adolescere 2018; VI (2): 6-14
Resumen
|
Palabras clave: Adolescencia; Vacunas; Calendarios de vacunaciones; Vacunas frente al virus del papiloma humano; Vacunas antimeningocócicas. |
Abstract
|
Key words: Adolescence; Vaccines; Vaccination schedules; Vaccines against human papillomavirus; Meningococcal vaccines. |
Introducción
Los progresos en el calendario pediátrico de vacunaciones sistemáticas en la última década afectan a los dos extremos de la edad pediátrica: por una parte, a la protección del recién nacido y del lactante menor de 3 meses, con la incorporación de nuevas vacunas en el calendario de la embarazada, y por otra, a las inmunizaciones del adolescente, que también se han incrementado por las nuevas vacunas autorizadas.
El calendario de vacunaciones del adolescente se ha enriquecido en los últimos años con la autorización de nuevas vacunas: dos vacunas triples bacterianas de baja carga antigénica del componente Bordetella pertussis (Tdpa3 y Tdpa5 [tétanos, difteria de carga antigénica reducida tipo adulto, tosferina con componentes acelulares de carga antigénica reducida], tricomponente y pentacomponente para la tosferina, respectivamente), una vacuna combinada dTpa3-VPI (virus de la poliomielitis inactivado tipo Salk), dos vacunas tetravíricas (sarampión, rubéola, parotiditis y varicela), tres vacunas frente al virus del papiloma humano (VPH) (bivalente, tetravalente y nonavalente), tres vacunas antigripales tetravalentes, y las vacunas frente a cinco serogrupos de Neisseria meningitidis (vacuna conjugada frente al serogrupo C, vacuna tetravalente conjugada frente a los serogrupos A, C, W, Y, y dos vacunas antimeningocócicas B). Estas 16 vacunas son necesarias para cumplimentar el calendario de vacunaciones sistemáticas, los calendarios incompletos y los calendarios de las situaciones especiales del adolescente.
La historia clínica debe contemplar antecedentes de vacunas recibidas, tipo, dosis y fechas de administración
La importancia de la inmunización del adolescente se ha de considerar en primer lugar en la historia clínica. La anamnesis debe contemplar los antecedentes de las vacunaciones recibidas, es decir, los tipos de vacunas, las dosis y las fechas de administración, con la finalidad de continuarlas o completar las que falten, y anotarlas o registrarlas correctamente en el carnet vacunal. Existen tres propuestas de calendario de vacunaciones sistemáticas del adolescente: la del Consejo Interterritorial del Sistema Nacional de Salud (SNS, 2018), en la que se basan los 17 calendarios de las comunidades autónomas y de las dos ciudades autónomas; la de la Asociación Española de Pediatría (AEP, 2018), que como sociedad científica que incluye la medicina de la adolescencia es la que consultan la mayoría de los pediatras; y una tercera, un calendario «de máximos», con las vacunas autorizadas y disponibles en el momento actual (2018) (Tabla I). Además, existe un cuarto calendario, el de los adolescentes no vacunados o insuficientemente inmunizados (Tabla II).
Las vacunaciones del adolescente en circunstancias especiales deben atenerse, en general, a las mismas recomendaciones y normas que en otras edades de la vida. Las situaciones más importantes son los pacientes con enfermedades crónicas, con trastornos de la inmunidad y las adolescentes embarazadas. Deben considerarse también en esta etapa de la vida, las recomendaciones de vacunación como profilaxis posexposición frente a enfermedades de transmisión sexual, así como las inmunizaciones del viajero.
Para mantener altas coberturas vacunales en la adolescencia, las vacunas deberían administrarse en los centros escolares
Las coberturas vacunales de los adolescentes en España correspondientes al año 2016, según datos del Ministerio de Sanidad, Política Social e Igualdad, son: a) sexta dosis de vacuna dT a los 14-16 años de edad: 82%; b) vacunación frente al VPH a los 11-14 años: 77,8%. Estas coberturas son más bajas, en todos los países, que las correspondientes a los primeros 2 años de la vida (entre el 95,4% y el 98%, según las vacunas, en España, en 2016), cuando el niño tiene mucho más contacto con el sistema sanitario y acude con más frecuencia y regularidad a las visitas de control del niño sano que más tarde en la adolescencia. Por esto es crucial que la vacunación del adolescente, para alcanzar y mantener unas altas coberturas vacunales, se realice en la escuela, como se ha demostrado, por ejemplo, con el programa de vacunación de la hepatitis B en el adolescente en Cataluña, durante 25 años. Además, la información prevacunal a padres y adolescentes por parte del pediatra y del personal de enfermería, y en general de todos los profesionales sanitarios, acerca de todas las vacunas, es un aspecto que debe ser priorizado y nunca hay que olvidar.
Vacunaciones de rescate
Al realizar la anamnesis vacunal al adolescente hay que interrogar sobre las vacunas y las dosis que ha recibido para verificar si el calendario de la comunidad donde reside está al día, y se le solicitará el carnet vacunal. Sin embargo, la vacuna triple vírica, la de la varicela y las vacunas de las hepatitis B y A han formado parte, en algún momento, de los calendarios del adolescente, pero ahora se incluyen en el calendario del lactante (hepatitis B) o del niño (triple vírica, varicela y en algunas comunidades hepatitis A), por lo que deberá confirmarse que se han administrado ya que durante un tiempo coexistieron o se solaparon en los dos calendarios.
La vacuna frente al VPH se administra en chicas a los 11-12 años, aunque es también aplicable en edades posteriores
La vacuna frente al VPH se administra a las chicas preferentemente a los 11-12 años porque se considera la edad óptima; la recomendación es también aplicable a edades posteriores, en caso de retraso en su administración, dados los beneficios que puede seguir aportando, tal como se indica en el calendario de la AEP y en el calendario «de máximos», por lo que se incluye en este apartado de las vacunaciones de rescate en la adolescencia; rescate que también debe ser considerado en la mujer adulta.
Vacuna triple vírica, vacuna de la varicela y vacuna tetravírica
El sarampión, la rubéola y la parotiditis son tres enfermedades cuya incidencia ha disminuido de forma importante desde 1987, por la introducción de la vacunación sistemática con la vacuna triple vírica en 1981, a los 12-15 meses de edad (Cataluña la había incluido en 1980 a los 12 meses de edad). En 1988, el Departamento de Sanidad y Seguridad Social de la Generalitat de Cataluña introdujo una segunda dosis de esta vacuna a los 11 años de edad para niños y niñas, sustituyendo a la de la rubéola que se administraba a las niñas. Esta estrategia fue seguida posteriormente por todas las comunidades autónomas, y figuró en el calendario del Consejo Interterritorial del SNS de 1995. Con esta inmunización se iniciaba el calendario universal (chicos y chicas) de vacunaciones del adolescente.
La segunda dosis se implantó con dos objetivos: aumentar la cobertura vacunal de la población al inmunizar a todos los niños susceptibles por no estar vacunados previamente o por disminuir el fallo vacunal primario (eficacia del 95%), y por otra parte reforzar la inmunidad al conseguir un efecto booster que aumenta el título de anticuerpos, con lo cual se logra una protección más duradera, sobre todo en los escasos casos de fallo secundario. En 1999 se acordó adelantar la segunda dosis a los 3-6 años de edad, preferentemente a los 3-4 años, como parte del plan para la eliminación del sarampión, con el fin de que no hubiera niños susceptibles en edad escolar. De esta manera, dejó de ser una vacuna del calendario del adolescente.
No obstante, en los últimos años se han producido brotes de sarampión en muchos países europeos, y también de parotiditis. En cuanto a la rubéola, hay que señalar la alta tasa de susceptibilidad en la población inmigrante en edad fértil, debido a que en sus países de origen la vacunación se ha realizado durante muchos años con la vacuna monovalente del sarampión.
La vacuna triple vírica forma parte del calendario entre las vacunas de recuperación del adolescente. La tetravírica se utilizará si hay
que vacunar de la varicela
En este momento, la vacuna triple vírica forma parte del calendario del adolescente entre las vacunaciones de recuperación, y cabe recordar que no existen vacunas monovalentes frente a las tres enfermedades. Hay que vacunar con dos dosis separadas en un intervalo de 1 mes, si no se han administrado previamente las dos dosis de vacuna triple vírica después de los 12 meses de edad. Si el niño ya había recibido una primera dosis después de esta edad, se administrará la dosis restante. Se utilizará la vacuna tetravírica si hay que vacunar también de la varicela.
En relación con los brotes de parotiditis, en los Estados Unidos se ha recomendado (enero de 2018), la administración de una tercera dosis de vacuna triple vírica en estas situaciones para las personas de alto riesgo que determinen las autoridades sanitarias.
La varicela es, en la actualidad, la enfermedad exantemática más frecuente en la población infantil en los países desarrollados, tras la disminución de la incidencia del sarampión y de la rubéola gracias a la inmunización sistemática con la vacuna triple vírica. Desde el calendario de 2005 hasta el de 2017 del Consejo Interterritorial del SNS, la vacuna de la varicela ha figurado en la adolescencia, a los 12 años, para quienes refieran no haber pasado la enfermedad ni haber sido vacunados con anterioridad con dos dosis. En el calendario de la AEP del año 2001 ya se incluyó a los 12-15 meses con un rescate a los 11-12 años. Se utilizará la vacuna tetravírica si hay que vacunar también del sarampión, la rubéola o la parotiditis.
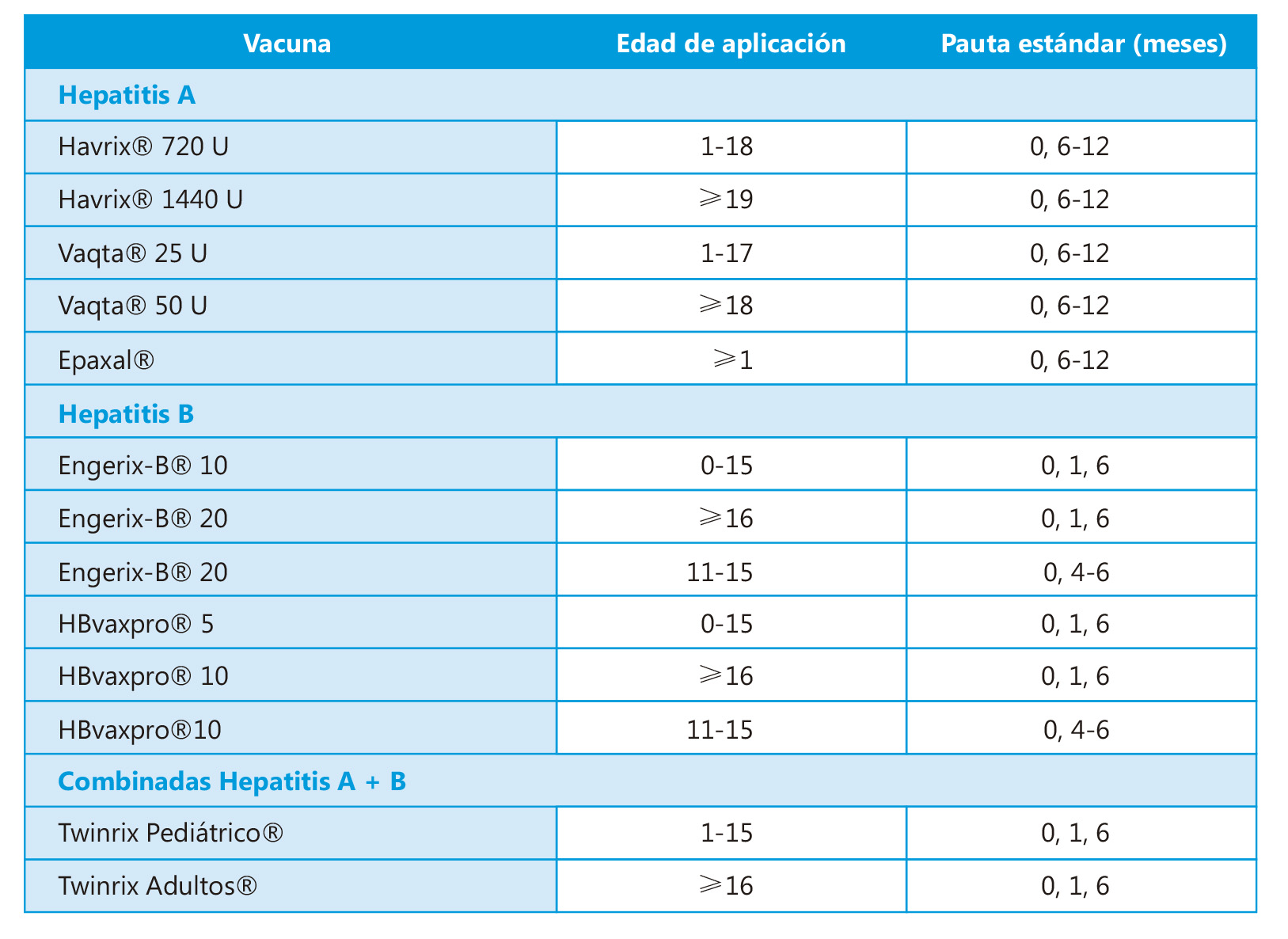
Vacunas antihepatitis B y A, y vacuna combinada hepatitis A+B
La infección por el virus de la hepatitis B es una de las causas más importantes de hepatitis aguda y crónica, cirrosis y carcinoma hepatocelular primario. El mayor riesgo de enfermedad crónica se observa cuando se contrae la infección en el periodo perinatal (70-90%), es más bajo en los menores de 5 años (20-50%) y aún más en los niños mayores y en los adultos (5-10%).
Es conveniente implantar la vacunación de la hepatitis B en la adolescencia, ya que el riesgo de infección se incrementa entre los 14 y 25 años
Cataluña fue la primera comunidad autónoma en iniciar un programa de inmunización frente a la hepatitis B. En 1985 se puso en marcha un programa dirigido a determinados grupos que tienen un alto riesgo de padecer la enfermedad, como los recién nacidos hijos de madres portadoras del virus (HBsAg positivas) y las personas en contacto íntimo (convivientes y parejas sexuales) con portadores crónicos. En 1986 se aprobó el programa de inmunización pasiva y activa de los recién nacidos hijos de madres HBsAg positivas. En 1990 se consideró que, para obtener un impacto eficaz y a corto plazo sobre la incidencia de la hepatitis B, era conveniente implantar la vacunación en la adolescencia, ya que el riesgo de infección por este virus es bajo durante la edad infantil, pero aumenta de manera considerable a partir de la adolescencia, entre los 14 y los 25 años de edad, con el inicio de las relaciones sexuales y las conductas de riesgo, tal como mostraban los resultados de las encuestas seroepidemiológicas realizadas en Cataluña. Durante el curso 1991-1992, hace ahora 25 años, se inició la vacunación antihepatitis B de los niños y niñas de 11-12 años en las escuelas, y se incorporó al calendario de inmunizaciones.
Posteriormente, la vacuna de la hepatitis B se introdujo en el calendario de inmunizaciones sistemáticas de todas las comunidades autónomas en el primer año de vida, con dos pautas: 0, 2 y 6 meses, o 2, 4 y 6 meses (desde 2006-2007 la pauta es 2, 4 y 11 meses). Canarias y Cataluña fueron las dos últimas comunidades que hasta el año 2002 mantuvieron una estrategia vacunal exclusiva en el adolescente (11-12 años) y en los recién nacidos hijos de madre portadora.
La hepatitis A es una enfermedad infectocontagiosa que en los niños casi siempre tiene un curso leve (asintomática o con manifestaciones inespecíficas moderadas, sin ictericia), mientras que en los adolescentes y los adultos es sintomática (ictericia) y de mayor gravedad. Su prevalencia varía de manera importante de unos países a otros en relación con las condiciones higiénicas, sanitarias y socioeconómicas de la población. A medida que estas mejoran, disminuye la seroprevalencia en la población infantil, lo cual origina un cambio en el patrón epidemiológico de la infección, caracterizado por un desplazamiento de la curva de prevalencia de anticuerpos hacia edades más avanzadas, que da lugar a un incremento paulatino de la población adulta joven susceptible, en la que la enfermedad es más grave.
Desde 1993 se comercializa en España la vacuna monovalente contra la hepatitis A, y desde 1997 la combinada contra las hepatitis A y B, que facilita su incorporación al calendario de inmunizaciones sistemáticas, como ha ocurrido en Cataluña desde el curso escolar 1997-1998, donde se desarrolla un programa piloto de vacunación contra las hepatitis A y B en las escuelas, a los 11-12 años de edad, sustituyendo a la vacuna monovalente de la hepatitis B. De esta forma, al reducirse la incidencia de la infección por el virus de la hepatitis A en la infancia también se prevendrá la enfermedad en los adultos que la adquieren de los niños. Este programa piloto finalizó cuando la primera cohorte de lactantes vacunados de hepatitis B a partir de los 2 meses de edad llegó a la adolescencia (curso 2014-2015); a partir de entonces se ha continuado solo con la vacuna de la hepatitis A y se ha incorporado al calendario de vacunaciones sistemáticas a los 15 meses y a los 6 años. Ceuta y Melilla también la tienen en su calendario en el segundo año de vida. El resto de las comunidades autónomas solo la administran a los grupos de riesgo. Las elevadas inmunogenicidad, seroprotección y efectividad de esta vacuna, como se ha demostrado en Cataluña en los últimos 20 años, junto con la eficiencia de la vacunación, la aconsejan mientras no sea una vacuna sistemática en la infancia. Además, según los últimos estudios publicados, en un futuro próximo es posible que se pueda administrar en una pauta de una sola dosis.
La vacunación puede realizarse, según los casos, con las vacunas monovalentes de las hepatitis B o A, o con la combinada de las hepatitis A+B.
Calendarios de vacunación del adolescente
Calendario del Consejo Interterritorial del Sistema Nacional de Salud (2018)
Se incluyen las siguientes vacunaciones:
- Vacuna frente al meningococo del serogrupo C a los 12 años.
- Vacuna frente al virus varicela-zóster a los 12 años, con dos dosis, en las personas que refieran no haber pasado la enfermedad ni haber sido vacunadas con anterioridad con dos dosis.
- Vacuna frente al VPH a los 12 años solo a las chicas.
- Vacuna Td (tétanos, difteria de carga antigénica reducida tipo adulto) a los 14 años.
Calendario de la Asociación Española de Pediatría (2018)
La vacuna del VPH se debe informar y recomendar también a los chicos
Se incluyen las siguientes vacunaciones sistemáticas:
- Vacuna Tdpa a los 12-18 años, preferiblemente a los 12-14 años.
- Vacuna frente al meningococo del serogrupo C a los 12 años.
- En el apartado dedicado a esta vacunación se recomienda dar información y la administración individualizada de la vacuna MenACWY para niños y adolescentes: a partir de los 14 años que vayan a residir en países donde la vacuna se indique a esa edad, como los Estados Unidos, Canadá, Reino Unido, Austria, Grecia e Italia; mayores de 6 semanas de vida, en caso de viaje a países con alta incidencia de enfermedad invasiva por los serogrupos incluidos en la vacuna; y mayores de 6 semanas de vida con factores de riesgo de enfermedad meningocócica invasiva (asplenia anatómica o funcional, déficit de factores del complemento, tratamiento con eculizumab, episodio previo de enfermedad invasiva por cualquier serogrupo y contactos de un caso índice de enfermedad invasiva por serogrupo A, W o Y). Se informará de la disponibilidad de las vacunas meningocócicas tetravalentes a los padres de los niños de 14 o más años que deseen ampliar en sus hijos, de forma individual, la protección frente al meningococo.
- Vacuna frente al VPH a las chicas, preferentemente a los 12 años, que se considera la edad óptima. La recomendación es también aplicable a edades posteriores, en caso de retraso en su administración, dados los beneficios que puede seguir aportando. Se debe informar y recomendar también a los chicos.
Calendario «de máximos» elaborado con las vacunas disponibles (2018)
Con las vacunas disponibles en España puede elaborarse un calendario, denominado «de máximos» (Tabla I), en el que figuran aquellas vacunas que se consideran recomendables para el adolescente, algunas financiadas por el SNS y otras no, ya que la recomendación individual no coincide siempre con la sistemática, debido sobre todo a criterios de eficiencia. La vacuna de la hepatitis A, presente en los calendarios de tres comunidades autónomas, se deberá administrar lo más precozmente posible. La vacuna antigripal anual se utilizará siempre en la forma tetravalente para obtener la máxima protección.
Vacuna frente al virus del papiloma humano
A finales de 2017 se cumplieron 10 años de la comercialización en España de las dos primeras vacunas frente al VPH, primero la tetravalente (VPH 6, 11, 16 y 18) en octubre de 2007, que ya había sido aprobada por la Food and Drug Administration en 2006, y luego la bivalente (VPH 16 y 18) en enero de 2008. Una tercera vacuna se comercializó en mayo de 2017, la nonavalente, que amplía el espectro al incluir cinco genotipos más (VPH 31, 33, 45, 52 y 58); la FDA la había autorizado en diciembre de 2014.
El 10 de octubre de 2007, el Consejo Interterritorial del SNS recomendó, e incluyó en el calendario de ese mismo año, la vacunación sistemática de las niñas de una cohorte, a elegir entre las de 11-14 años de edad por cada comunidad autónoma en función de sus necesidades, prioridades y logística de los programas de vacunación, con un plazo de implantación hasta el año 2010. Tres comunidades iniciaron la vacunación a finales de 2007 y el resto lo hicieron durante 2008. La vacuna está en el calendario de la AEP desde 2008. En noviembre de 2017, Cataluña incorporó en su calendario la forma nonavalente, mientras que en el resto de las comunidades autónomas se utiliza la bivalente o la tetravalente.
La vacuna del VPH se recomienda en pauta de dos dosis desde los 9 años hasta los 13-14 años, y vacunación sistemática
del varón en algunos países
En estos 10 años de disponibilidad de vacuna frente al VPH (que junto con la vacuna de la hepatitis B son las únicas que previenen un cáncer) se ha progresado en su conocimiento y se han producido avances importantes en las estrategias de vacunación y en las indicaciones y recomendaciones: adelanto de la edad de vacunación en el calendario, pautas de dos dosis desde los 9 hasta los 13-14 años, vacunación sistemática del varón en algunos países, inmunización de la mujer más allá de la adolescencia, implementación de programas de vacunación en países en desarrollo, prevención de otras neoplasias, recomendaciones de vacunación para poblaciones de riesgo elevado de infección por el VPH, evidencia científica del impacto y la efectividad de la vacunación, y confirmación de su seguridad con más de 270 millones de dosis administradas, como ya se había observado en los ensayos clínicos.
La vacuna del VPH previene al varón de las verrugas anogenitales y los cánceres de ano, pene, escroto y orofaringe
El cambio más importante en el calendario de máximos de la vacuna frente al VPH es la universalidad, es decir, la recomendación a chicos y chicas. La infección producida por el VPH es una verdadera enfermedad pandémica, por ser universal y porque afecta a mujeres y hombres a lo largo de toda la vida y en todo el mundo. La vacunación sistemática en el varón ya se ha implementado en 13 países. Esta inmunización previene en el hombre las verrugas anogenitales y los cánceres de ano (indicaciones ya incluidas en la ficha técnica de las vacunas tetravalentes y nonavalentes), pene, escroto y orofaringe, pero la gran justificación de la vacunación universal es la prevención de la transmisión sexual de la infección, ya que tanto el hombre como la mujer están implicados en la cadena epidemiológica y pueden ser portadores asintomáticos, transmisores y enfermos. La vacunación universal disminuirá la tasa de transmisión del VPH, aumentará la protección de grupo y conseguirá la equidad vacunal.
El papel de los profesionales de la salud vinculados con la vacunación en la adolescencia (pediatras y enfermería pediátrica) y la edad adulta (médicos de familia y enfermería) está siendo primordial en la información y la sensibilización sobre las infecciones producidas por el VPH y su prevención, así como en la difusión y la aplicación de la vacunación, que en 2016 ha alcanzado en España una cobertura del 77,5% (algo inferior a la del año anterior). Si queremos disminuir la incidencia del cáncer relacionado con el VPH, debemos esforzarnos todos en aumentar las coberturas vacunales y lograr, con la vacunación sistemática de los varones, una inmunización universal.
Vacunas meningocócicas: frente al serogrupo B y tetravalente ACWY
La epidemiología de la enfermedad meningocócica en España, y en Europa en general, con diferencias según los países, ha experimentado cambios importantes en la última década. Por una parte, se confirma una disminución marcada de la incidencia (alrededor del 0,6/100.000 habitantes en España en 2016), y en cuanto a la distribución por serogrupos, el B continúa siendo el más frecuente, pero se ha producido una emergencia del W y del Y, sobre todo del primero, en el Reino Unido y en los países escandinavos, respectivamente. La distribución por serogrupos en el Reino Unido en 2016 fue: B 52%, W 28% e Y 13%. A partir de 2015 empezó a detectarse en España un aumento progresivo del número de casos de enfermedad meningocócica por el serogrupo W, aunque durante 2017 parece haberse estabilizado (datos provisionales); en la temporada 2015-2016, la distribución fue la siguiente: B 57,8%, W 10% e Y 6,4%.
El origen de la emergencia del serogrupo W fue que en el año 2000 se produjo un brote epidémico de enfermedad invasiva por este serogrupo en la peregrinación anual a La Meca. El serotipo implicado, ST-11CC82, muy virulento, se extendió a través de dos linajes diferentes a varios países africanos y a Latinoamérica, y desde allí al Reino Unido y otros países europeos.
El serogrupo Y también ha aumentado en algunos países de la Unión Europea, especialmente en los nórdicos, entre los años 2007 y 2011. En el periodo 2007-2009 el incremento fue del 42%, con un porcentaje de este serogrupo del 34%, el 25% y el 15% en Suecia, Noruega y Finlandia, respectivamente.
Otro dato relevante en la epidemiología de la enfermedad meningocócica en relación con el adolescente es que, en su distribución por edades, después del pico de máxima incidencia del primer año de vida y los menores de 5 años, se sitúa el grupo de 15 a 24 años (adolescentes y adultos jóvenes). Además, el número de casos en la adolescencia representa una importante proporción del total de casos, que oscila entre el 15% en Portugal y el 32% en Noruega. Por último, hay que destacar que el mayor porcentaje de portadores nasofaríngeos de meningococo, primer estadio en la transmisión de la infección, se observa en la adolescencia, con un pico máximo a los 19 años (23,7%), lo que convierte a este grupo en el primer transmisor de la infección, además de entre los adolescentes, a los niños pequeños y a las personas mayores.
En el Reino Unido, las autoridades sanitarias decidieron incluir en el calendario una dosis de vacuna conjugada tetravalente ACWY en lugar de la tercera dosis de vacuna meningocócica C a los 14 años. En España, por el momento, las autoridades sanitarias, teniendo en cuenta la situación epidemiológica actual y los criterios de eficiencia de la vacunación, solo han establecido recomendaciones para los grupos de riesgo, entre los que se incluyen los viajeros a países con elevada incidencia de los serogrupos W e Y, para quienes la vacuna está financiada.
En nuestro país, las vacunas meningocócicas sólo han establecido recomendaciones para los grupos de riesgo (viajeros a países con incidencia de los serogrupos W e Y)
En el calendario de la AEP se añade, además, que se informará de la disponibilidad de las vacunas meningocócicas tetravalentes a los padres de los niños de 14 o más años que deseen ampliar en sus hijos, de forma individual, la protección frente al meningococo.
En el calendario «de máximos» se incluye esta vacuna entre los 12 y los 16 años, de preferencia a los 14 años, en lugar de la tercera dosis de la vacuna meningocócica C. La sustitución de esta vacuna del calendario oficial se deberá explicar y razonar a los padres. Debido a que se ha observado una disminución en los títulos de anticuerpos con el paso del tiempo, se puede considerar una dosis de recuerdo en los sujetos vacunados que tengan alto riesgo de exposición a la enfermedad meningocócica, que en los Estados Unidos se indica a los 5 años. En la situación de un adolescente que hubiera sido vacunado a los 12 años con la vacuna frente al serogrupo C y que viajase a un país donde se recomienda la vacuna tetravalente, se le debería administrar esta vacuna.
La otra vacuna antimeningocócica del calendario del adolescente es la del serogrupo B. En España, por el momento, las autoridades sanitarias, teniendo en cuenta la situación epidemiológica actual (y hay que recordar que es el primero en frecuencia, claramente por delante de los serogrupos W e Y) y los criterios de eficiencia de la vacunación, solo han establecido recomendaciones para los grupos de riesgo, en los cuales la vacuna está financiada.
En el calendario de la AEP esta vacuna se incluye como sistemática, pero en el primer año de vida. En el calendario «de máximos» se recomienda, basándose en las características epidemiológicas antes mencionadas, a los 14-18 años en una pauta de dos dosis separadas por un intervalo de 1 mes.
Calendario de los adolescentes no vacunados o insuficientemente inmunizados
En la Tabla II se indica el número de dosis que requiere el adolescente que presenta un calendario de vacunaciones incompleto o que quiere iniciar las inmunizaciones. Son las llamadas pautas de rescate o aceleradas. Al cumplimentar este calendario hay que tener en cuenta siempre la edad mínima de aplicación de cada vacuna y los intervalos mínimos entre dosis, y el principio general de la vacunología: «dosis administrada, dosis válida; no hay que reiniciar pautas, sino continuarlas y completarlas, con independencia del intervalo transcurrido desde la última dosis».
En la vacunación con Td (se indican tres a cinco dosis en la tabla), una vez completada la primovacunación con tres dosis se recomienda utilizar la vacuna Tdpa en una de las dosis de recuerdo, aunque existen pautas que ya la utilizan en la tercera dosis de la primovacunación. Para que un adulto primovacunado en la adolescencia, o más tarde, se considere completamente inmunizado frente al tétanos, debe haber recibido al menos cinco dosis de vacunas con toxoide tetánico en su vida, por lo que, tras la primovacunación, deberá recibir dos dosis de refuerzo separadas por 10 años.
La pauta de vacunación frente al VPH a partir de los 15 años es de tres dosis, en los meses 0, 1 y 6
En la vacunación frente al VPH (se indican dos o tres dosis en la tabla), el número de dosis varía según la edad del adolescente y el preparado vacunal. Para la vacuna bivalente, la pauta de vacunación para los adolescentes de 9 a 14 años incluye dos dosis, la segunda administrada a los 6 meses de la primera (flexible entre 5 y 13 meses). La pauta de vacunación a partir de los 15 años es de tres dosis en los meses 0, 1 y 6. Para la vacuna tetravalente, la pauta de vacunación entre los 9 y los 13 años es también de dos dosis, administradas en los meses 0 y 6, mientras que para la nonavalente el intervalo de edad es de 9 a 14 años. La pauta de vacunación posteriormente es de tres dosis en los meses 0, 2 y 6. En las personas con inmunodepresión se recomienda usar siempre la pauta de tres dosis, independientemente de la edad.
CONCLUSIONES
La vacunación del adolescente forma parte de las estrategias preventivas incluidas en el plan de salud de este periodo de la vida. Al comienzo de la adolescencia (10 años), el pediatra debe incluir en la visita de control, además de las exploraciones y las pruebas de cribado correspondientes a la edad, consejos y educación para la salud, y en relación con las inmunizaciones:
- Asegurar la vacunación frente a la hepatitis B de los no vacunados previamente; la vacunación triple vírica de los no vacunados con dos dosis; la vacunación antimeningocócica C de los no inmunizados con una vacuna conjugada, al menos con una dosis después del año de edad; y la vacunación de la varicela a los susceptibles, es decir, a los no vacunados o que solo han recibido una dosis, o que no han padecido la enfermedad.
- Iniciar de forma precoz, a los 11 años de edad (se puede comenzar a partir de los 9 años), la vacunación frente al VPH, y hacer una vacunación de rescate de todas las adolescentes mayores de esta edad no vacunadas, preferentemente con vacuna nonavalente.
- Recomendar el calendario «de máximos», es decir, el que ofrece la máxima protección con las vacunas disponibles: una sexta dosis de vacuna frente a la tosferina, con la vacuna dTpa en lugar de la dT, hepatitis A, vacunas antimeningocócicas B y ACWY, vacunación universal frente al VPH, incluyendo por tanto a los varones, y vacunación antigripal anual.
- Registrar en un carnet las vacunas administradas, que el adolescente llevará siempre consigo y que pondrá en conocimiento del médico de familia cuando este se haga cargo de su asistencia.
Tablas y figuras
Tabla I. Calendario «de máximos» de vacunaciones del adolescente
|
|
|
|
|
|
|
Tdpa: tétanos, difteria de carga antigénica reducida tipo adulto, tosferina con componentes acelulares de carga antigénica reducida; VPH: virus del papiloma humano.
Tabla II. Calendario del adolescente (10-19 años) no vacunado: número de dosis recomendadas
|
Vacuna |
Nº dosis |
|
Hepatitis B |
3 |
|
Tétanos, difteria de baja carga antigénica |
3-5 (una dosis de Tdpa) |
|
Poliomielitis |
3 |
|
Sarampión, rubéola, parotiditis |
2 |
|
Varicela |
2 |
|
VPH |
2-3 (según la edad) |
|
Meningococo B |
2 |
|
Hepatitis A |
2 |
|
Meningococo ACWY |
1-2 (según el riesgo) |
Tdpa: tétanos, difteria de carga antigénica reducida tipo adulto, tosferina con componentes acelulares de carga antigénica reducida; VPH: virus del papiloma humano.
Bibliografía
1. Comité Asesor de Vacunas de la Asociación Española de Pediatría. Calendario de Vacunaciones de la Asociación Española de Pediatría. Razones y bases de las recomendaciones 2018. [Internet]. Madrid: AEP; 2018. [Consultado el 31 Ene 2018]. Disponible en: http://vacunasaep.org/sites/vacunasaep.org/files/calvacaep2018-razones-y-bases.pdf.
2. Comité Asesor de Vacunas de la Asociación Española de Pediatría. Calendario de vacunaciones de rescate o acelerados 2018. [Internet]. Madrid: AEP; 2018. [Consultado el 31 Ene 2018]. Disponible en: http://vacunasaep.org/sites/vacunasaep.org/files/calvacaep_2018_acelerados_tablas.pdf
3. Consejo Interterritorial del Sistema Nacional de Salud. Calendario común de vacunación infantil. Calendario recomendado 2018. [Consultado el 31 Ene 2018]. Disponible en: http://www.msssi.gob.es/profesionales/saludPublica/prevPromocion/vacunaciones/Calendario2018.htm.
4. European Centre for Disease Prevention and Control. Expert opinion on the introduction of the meningococcal B (4CMenB) vaccine in the EU/EEA. Stockholm: ECDC; 2017.
5. Comité Asesor de Vacunas de la Asociación Española de Pediatría. Fichas técnicas de vacunas. [Consultado el 31 Ene 2018]. Disponible en: http://vacunasaep.org/profesionales/fichas-tecnicas-vacunas.
6. Folaranmi T, Rubin L, Martin SW, Patel M, MacNeil JR. Use of serogroup B meningococcal vaccines in persons aged ≥10 years at increased risk for serogroup B meningococcal disease: recommendations of the Advisory Committee on Immunization Practices, 2015. MMWR Morb Mortal Wkly Rep. 2015;64:608-12.
7. MacNeil JR, Rubin L, Folaranmi T, Ortega-Sánchez IR, Patel M, Martin SW. Use of serogroup B meningococcal vaccines in adolescents and young adults: recommendations of the Advisory Committee on Immunization Practices, 2015. MMWR Morb Mortal Wkly Rep. 2015;64:1171-6.
8. MacNeil JR, Rubin L, McNamara L, Briere EC, Clark TA, Cohn AC.Use of MenACWY-CRM Vaccine in Children Aged 2 Through 23 Months at Increased Risk for Meningococcal Disease: Recommendations of the Advisory Committee on Immunization Practices, 2013. MMWR Morb Mortal Wkly Rep. 2014;63:527-30.
9. Moraga Llop FA. Novedades en vacunología 2016-2017. En: Campins Martí M, Moraga Llop FA, editores. Vacunas 2017. Madrid: Undergraf; 2017. p. 201-16.
10. Moraga Llop FA. Diez años de vacunación frente al virus del papiloma humano. De la dermatología a la oncología a través de la infectología. An Pediatr (Barc). 2018. https://doi.org/10.1016/j.anpedi.2017.12.013.
11. Moraga-Llop F, Hidalgo Vicario MI. Calendario vacunal del adolescente: preguntas y respuestas. Adolescere. 2013;XII:5-23.
12. Moreno-Pérez D, Álvarez García FJ, Álvarez Aldeán J, Cilleruelo Ortega MJ, Garcés Sánchez M, García Sánchez N, et al. Calendario de vacunaciones de la Asociación Española de Pediatría (CAV-AEP): recomendaciones 2018. An Pediatr (Barc). 2018;88:53.e1-9.
13. Ortega Páez E, Esparza Olcina MJ. La edad óptima para vacunar con la vacuna conjugada antimeningocócica ACWY es entre los 12 y los 15 años. Evid Pediatr. 2017;13:50.
14. Patton ME, Stephens D, Moore K, MacNeil JR. Updated recommendations for use of MenB-FHbp serogroup B meningococcal vaccine — Advisory Committee on Immunization Practices, 2016. MMWR Morb Mortal Wkly Rep. 2017;66:509-13.
15. The Society for Adolescent Health and Medicine. Adolescent consent for vaccination: a position paper of the Society for Adolescent Health and Medicine. J Adolesc Health. 2013;53:550-3.
16. Schneyer RJ, Yang C, Bocchini Jr JA. Immunizing adolescents: a selected review of recent literature and US recommendations. Curr Opin Pediatr. 2015;27:405-17.