Sesión III Actualización: Vacunación en el adolescente. ¿Hacia un calendario de máximos?
Sesión III Actualización: Vacunación en el adolescente
Vacunación en el adolescente ¿Hacia un calendario de máximos?
I.Oiz Urriza, I.Rivero Calle.
Hospital Clínico Universitario de Santiago de Compostela
Adolescere 2023; XI (2): 47-57
Resumen
|
La adolescencia es una etapa de la vida cuyas características específicas y de forma de vida hacen que su cobertura vacunal sea subóptima. El presente artículo tiene como objetivo mostrar las recomendaciones vacunales actuales correspondientes a Neisseria meningitidis, virus del papiloma humano en ambos sexos, SARS-CoV2, tosferina, hepatitis A y gripe. Palabras clave: Adolescente; Vacunación; Virus del papiloma humano; Neisseria meningitidis, Serogrupo B; Serogrupo ACWY; Gripe; Tos ferina. |
Abstract
|
Adolescence is a stage of life whose specific characteristics and lifestyle make their vaccination coverage suboptimal. The aims of these article is to show current vaccination recommendations for Neisseria meningitidis, human papillomavirus in both sexes, SARS-CoV2, whooping cough, hepatitis A and influenza. Key words: Adolescent; Vaccination; Human papilloma virus; Neisseria meningitidis; Serogroup B; ACWY serogroup; Flu; Whooping cough. |
En la transición de la atención pediátrica a la atención médica del adulto que se da entre los 14 y 16 años, una organización deficiente puede condicionar que no se complete adecuadamente el calendario de vacunaciones
La población adolescente tiene ciertas peculiaridades que deben tenerse en cuenta para abordar de forma realista el presente y el futuro de la vacunación de nuestros jóvenes. Dado que desconocen sus necesidades de salud, acuden menos a la consulta y, por lo tanto, sus coberturas vacunales son menores. A esto se suma la transición de la atención pediátrica a la atención médica del adulto que se da entre los 14 y 16 años, cuya organización deficiente puede condicionar que no se complete adecuadamente el calendario de vacunaciones. Además, se trata de una etapa de numerosos viajes por intercambios, formación o turismo y de grandes cambios: un periodo problemático y de alto riesgo, pues, aunque conocen los riesgos, actúan como si estos no existieran.
Distintas sociedades pediátricas proponen una serie adicional de vacunas: meningococo B, VPH en ambos sexos, SARS-COV-2, tos ferina, hepatitis A, gripe y el rescate en no vacunados con varicela/TV/hepatitis B, más allá de las actualmente vigentes
A pesar de que la comisión interterritorial de vacunación tiene un calendario de vacunación que contempla específicamente a los adolescentes, distintas sociedades pediátricas de España (SEMA, AEP, AEPap, AEV, SEIP, SEMERGEN, SEMG, SEPEAP, SEUP) proponen una serie adicional de vacunas que tienen indicación a juicio del profesional que atiende al adolescente, o una recomendación sujeta a determinadas circunstancias (viajes, factores de riesgo) como son: meningococo B, VPH en ambos sexos, SARS-COV-2, tosferina, hepatitis A, gripe y el rescate en no vacunados con varicela/TV/hepatitis B, más allá de las actualmente vigentes (Td a los 14 años, Men ACWY a los 12 años, VPH a los 12 años y TV, hepatitis B, VVZ en personas susceptibles o no vacunadas con anterioridad)(1). (Ver Figuras 1 y 2).
Neisseria meningitidis serogrupo B
Las tasas de incidencia acumulada de enfermedad meningocócica invasiva (EMI) en nuestro país en los periodos comprendidos entre la semana 41 de 2022 y la semana 14 del 2023 son de 0,33 casos por cada 100.000 habitantes, siendo las franjas de edad con mayor número de casos, los lactantes menores de un año, niños entre 1-4 años y el periodo de adolescencia. Las comunidades autónomas con mayor incidencia acumulada son Cataluña, Valencia y Andalucía, siendo esta última la que acumula mayor letalidad (17,2 % de los casos)(2).
El número total de casos de enfermedad meningocócica invasiva en nuestro país se ha multiplicado por tres en esta última temporada 2022-2023 respecto a la misma temporada del año previo 2021-2022
Llama la atención que el número total de casos en nuestro país se ha multiplicado por tres en esta última temporada 2022-2023 respecto a la misma temporada del año previo 2021-2022 y que los serotipos B e Y se han duplicado, afectando especialmente a la primera infancia, mientras que el serotipo W se ha multiplicado por 4, afectando mayoritariamente a la población adolescente(2).
A pesar de que los lactantes y niños menores de 5 años son los que presentan mayor incidencia de enfermedad meningocócica invasiva(3) (EMI) debido a la inmadurez de su sistema inmune(4), un 17 % de los casos ocurren en la población de entre 15 y 24 años(5) y hasta un 24 % de los adolescentes son portadores de la bacteria causante de la enfermedad(6); por lo que el riesgo “0” no existe.
Vacunas frente a Meningococo B
A día de hoy, disponemos de dos vacunas frente a meningococo B con posible aplicación en la población adolescente(7):
- Bexsero®-4CMenB: vacuna compuesta por 4 antígenos, con posibilidad de ser administrada desde las 8 semanas de vida, datos de inmunogenicidad de hasta 7,5 años; y seguridad y eficacia demostrada en grupos especiales de alto riesgo (asplénicos, afectos de déficit del complemento o usuarios de tratamiento con eculizumab).
- Trumenba®-rLP٢٠٨٦: vacuna compuesta por dos variantes de un antígeno, con posibilidad de ser administrada a partir de los ١٠ años de edad y datos de persistencia de inmunidad de hasta ٤ años.
Ambas han demostrado su seguridad y eficacia en su desarrollo clínico, y ampliamente, su efectividad y seguridad en estudios de vida real(8); incluyendo en España, donde la efectividad vacunal para prevenir EMI con pauta completa de 4CMenB fue del 76 % por cualquier serogrupo y del 71 % para meningococo B. También mostró una alta efectividad contra EMI por serogrupos no B (92 %), aunque debe tenerse en cuenta que la efectividad de la vacunación completa es menor después de los 2 años y con esquemas de vacunación que comenzaron a partir de los 2 años(9). Sin embargo, no existen datos disponibles sobre la intercambiabilidad de ambas vacunas frente a meningococo B(7).
Logrando una cobertura vacunal adecuada en la adolescencia para el meningococo B se lograría una protección directa frente al meningococo B, una protección cruzada frente a otros serogrupos no B, protección directa y cruzada frente a meningococos no encapsulados causantes de uretritis multirresistentes y protección cruzada frente a Neisseria gonorrea
Por otro lado, de acuerdo al estado actual del conocimiento sobre la dinámica de la infección meningocócica y la estrategia vacunal se puede afirmar que con vacunas frente a meningococos ACWY podemos buscar protección directa y/o indirecta y con vacunas frente a meningococo B solo podemos buscar protección directa(10), dado que no se ha demostrado efecto en el portador, ni reducción de la carga de colonización nasofaríngea. Adicionalmente, y de forma muy interesante con la vacuna 4CMenB, se ha visto que con esta vacunación además de lograrse una protección directa frente al meningococo B, se podría conseguir una protección cruzada frente a otros serogrupos no B, protección directa y cruzada frente a meningococos no encapsulados causantes de uretritis multirresistentes y protección cruzada frente a Neisseria gonorrea(11,12).
Todo ello se embebe en el reto de erradicación de la meningitis bacteriana para 2030 siguiendo los objetivos de la OMS.
Virus del Papiloma Humano (VPH)
La infección por VPH es la enfermedad de transmisión sexual más frecuente en nuestro medio, siendo el 80 % de los individuos sexualmente activos potenciales transmisores del virus. Hay más de 200 tipos de VPH de los cuales al menos 40 pueden infectar el área anogenital estando algunos de ellos directamente relacionados con el desarrollo de neoplasias, siendo las más frecuentes las verrugas genitales, las displasias y cánceres cervicales de distinto grado y los cánceres de cabeza y cuello.
Existen 3 grandes grupos de vacunas frente al VPH: la bi-valente (Cervarix®, AOS4-AL) que cubre los serotipos 16 y 18, la cuatri-valente (Gardasil®, AAHS 250) que también incluye los serotipos 6 y 11 y la nona-valente (Gardasil 9®, AAHS 500) que abarca los serotipos 6, 11, 16, 18, 31, 33, 45, 52 y 58.
Aunque la vacunación en las mujeres adolescentes ya está estandarizada y financiada por el Sistema Nacional de Salud, en el caso de los varones, la incorporación de la vacuna está aún en proceso y no faltan las razones que justifiquen el beneficio que ofrece su uso en ambos sexos(13):
- Fracción de enfermedad oncológica relacionada con el VPH en el varón: Se diagnostican alrededor de 690.000 casos de cánceres relacionados con VPH en hombres y mujeres cada año en el mundo; de los cuales, en nuestro medio, el 25 % corresponden al varón, siendo los más frecuentes el cáncer de orofaringe, anal y peneano.
- Cáncer de cabeza y cuello relacionado con el VPH: Los varones tienen un mayor riesgo de infección y de ciertos cánceres relacionados con VPH, estando el ADN del virus presente en el 20-30 % de los carcinomas de orofaringe y en más del 50 % de los carcinomas de amígdalas.
- Cáncer de cabeza y cuello en aumento, sobre todo en varones: El carcinoma de células escamosas de la orofaringe en los hombres ha superado al cáncer de cuello uterino en las mujeres como el cáncer asociado al VPH más común en la población general en determinados países como EE.UU.
- Cáncer anal en aumento, sobre todo en varones: La incidencia del carcinoma anal de células escamosas está aumentando en los hombres en EE.UU y en otros países con ingresos económicos altos.
- No hay cribado de las otras patologías oncológicas relacionadas con VPH: Los CDC no recomiendan el cribado para los cánceres de ano, pene u orales en hombres. Sin embargo, los datos sobre poblaciones de alto riesgo de hombres que tienen sexo con hombres (HSH) y varones VIH positivos sugieren que estas poblaciones pueden beneficiarse del cribado.
- Impacto poblacional de la vacunación sobre las verrugas genitales: Se ha observado una disminución del 67 % en mujeres de entre 15 y 19 años y en el 48 % de los varones gracias a la implementación de la vacunación frente a VPH en mujeres. Por otro lado, en un estudio de cohortes realizado en España, se observa una reducción del 61 % en la tasa de incidencia de las verrugas genitales en las mujeres de entre 16-19 años, una tendencia decreciente en hombres de entre 16-22 años (aunque no significativa); y un incremento de otras infecciones de transmisión sexual como el herpes genital.
- La inmunidad de grupo generada con la vacunación solo de chicas es incompleta para el varón: Por un lado, existe un promedio de un 20-25 % de chicas no vacunadas en nuestro medio y que son potenciales transmisoras del VPH a los chicos heterosexuales. En los países que incluyen la vacunación frente al VPH y aquellas con prácticas heterosexuales, pueden estar protegidas de forma indirecta con la vacunación del varón. Sin embargo, el efecto de inmunidad de grupo observado en algunos países (como Australia) no se ha podido observar en países europeos que han estudiado este efecto; y además, los hombres que tienen sexo con hombres no pueden beneficiarse de la inmunidad de grupo que se puede generar vacunando solo a las chicas.
- Ayuda a la erradicación global de la infección por VPH: No debemos olvidar que los chicos son los mayores transmisores del virus a nivel mundial; pero además, su vacunación aporta: un beneficio directo sobre la prevención de los cánceres ligados al VPH (orofaríngeo, ano, pene y escroto) así como de las verrugas genitales, y un beneficio indirecto contribuyendo a la disminución y al control de esta infección de transmisión sexual y a la protección de las mujeres no vacunadas y de los HSH no vacunados.
- Igualdad-equidad sexual dado que, si la vacuna protege frente al cáncer relacionado con el VPH en ambos sexos, es ético incluir a ambos sexos en las recomendaciones.
- Autorización para el empleo de las vacunas VPH en el varón y experiencia en otros países:
El carcinoma de células escamosas de la orofaringe en los hombres ha superado al cáncer de cuello uterino en las mujeres como el cáncer asociado al VPH más común en la población general en EE.UU.
La inmunidad de grupo generada con la vacunación solo de chicas es incompleta para el varón
a) Inmunogenicidad en varones similar a las obtenidas en la mujer.
i. La inmunogenicidad no fue inferior en varones heterosexuales frente a mujeres y los GMT para los 9 tipos de VPH de la vacuna fueron más bajos en HSH en comparación con hombres heterosexuales y mujeres.
b) Eficacia frente a lesiones genitales externas, lesiones intraepiteliales peneanas (PIN) y anales (AIN) en hombres de 16 a 26 años.
i. VPH4v es muy eficaz en la prevención de lesiones genitales externas, verrugas genitales y PIN relacionados con VPH 6/11/16/18 en hombres, tuvo una eficacia del 74,9 % para prevenir AIN de alto grado relacionada con el VPH 6/11/16/18 en HSH; y brindó protección contra la enfermedad anogenital relacionada con el VPH 6/11/16/18 en hombres durante 10 años.
c) Disponemos de datos de un posible impacto en la reducción de la enfermedad y efectividad.
La vacunación reduce el porcentaje de infección VPH persistente oral, genital y anal, así como las lesiones anales preneoplásicas de alto grado. Además, podría proteger contra la progresión de cánceres orales, ya que pueden inhibir eficazmente la infección por VPH
i. La vacunación reduce el porcentaje de infección por VPH persistente oral, genital y anal, así como las lesiones anales preneoplásicas de alto grado. Además, podría proteger contra la progresión de cánceres orales, ya que pueden inhibir eficazmente la infección por VPH.
Ya hay 47 países con vacunación sistemática frente a VPH en varones, 19 en Europa.
SARS-CoV2
Desde el inicio de la pandemia en 2019 la infección por SARS-CoV2 también ha afectado a la población pediátrica, objetivándose en España un 8,9 % de requerimiento de ingreso hospitalario en casos reportados en menores de 9 años y un 13 % en los adolescentes de entre 10 y 19 años (14).
Existen en España 3 vacunas aprobadas por la EMA para uso pediátrico(15) cuya cobertura con una dosis ha sido del 53,5 % en los niños de entre 5 y 11 años; y en los adolescentes de entre 12 y 19 años, hasta un 86,3 % tienen la pauta completa de vacunación(16).
- Comirnaty (mRNA): monovalente (original) cuyo uso está autorizado desde los 6 meses como vacunación primaria y bivalente (original + ómicron) desde los 5 años como refuerzo y 12 años como vacunación primaria.
- Spikevax (mRNA): monovalente (original) aprobado desde los 6 meses como vacunación primaria y de refuerzo a partir de los 6 años y bivalente (original + ómicron) como vacunación primaria desde los 12 años.
- Nuvaxovid (proteínas adyuvada) solamente autorizada como vacunación primaria a partir de los 12 años y como refuerzo desde los 6 años.
Entre los beneficios de la vacuna del SARS-CoV2 en la edad pediátrica: evitan hospitalizaciones y alteraciones de la vida social de niños y adolescentes, contribuyen a disminuir la transmisión comunitaria y evitan casos en otras edades
Puede decirse que los beneficios de la vacunación en la edad pediátrica son patentes ya que, aunque los síntomas son menos frecuentes y por lo general más leves que en la población adulta, puede darse la hospitalización y el síndrome de inflamación sistémica pediátrica (SIMP). Además, la eficacia y seguridad de las vacunas han sido probadas y existen beneficios directos e indirectos ya que evitan hospitalizaciones y alteraciones de la vida social de niños y adolescentes, contribuyen a disminuir la transmisión comunitaria, y evitan casos en otras edades.
Tosferina
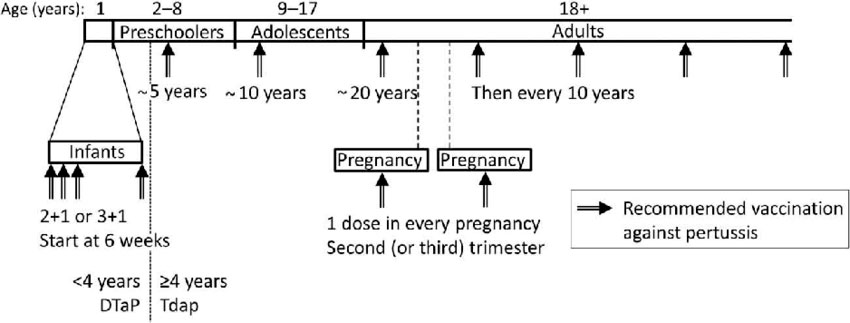
El Comité Asesor de Vacunas de la Asociación Española de Pediatría (CAV-AEP) recomienda la administración de Tdpa a los 12-14 años, en vez de solo Td, porque para conseguir un adecuado control de la tosferina, se requieren elevadas coberturas vacunales y un esquema de vacunación completo desde el lactante al adolescente y adulto(17) (Ver Figura 3). Para ello se propone la siguiente pauta de vacunación: durante el primer año 2+1 ó 3+1 iniciando a las 6 semanas de vida (vacuna DTPa), Tdpa a los 5, 10 y a los 20 años; y a partir de ahí, cada 10 años, sin olvidar la administración de una dosis en cada embarazo entre el 2º y 3er trimestre de gestación(18).
Hepatitis A
A pesar de que la vacunación frente al virus de la hepatitis A (VHA) no está indicada en todos los niños, sí lo está en condiciones de riesgo de infección o exposición como pueden ser los niños con infección por VIH o aquellos que padecen una enfermedad hepática crónica. También se incluyen en la vacunación recomendada para el VHA los usuarios de drogas por vía parenteral, aquellos con conductas sexuales de riesgo (prostitución, HSH) y personal que viaja a zonas endémicas.
No obstante, esta situación es distinta en Ceuta y Melilla, donde la vacunación frente a VHA es obligatoria desde el año 2000 a los 15 y 24 meses; y en Cataluña, donde lo es a los 15 meses y 6 años desde el 2015.
Según las recomendaciones del CAV-AEP, la vacunación exclusiva a la población de riesgo tiene muy poco impacto en la incidencia de la enfermedad. Además, el VHA es potencialmente erradicable, al tener un reservorio exclusivo humano, no haber infección crónica por VHA y una muy alta efectividad vacunal incluso con una sola dosis. Es por eso que la vacunación universal a niños y adolescentes, sería la estrategia óptima para la eliminación y control de la enfermedad.
Según las recomendaciones del CAV-AEP la vacunación exclusiva de Hepatitis A a la población de riesgo tiene muy poco impacto en la incidencia de la enfermedad. La vacunación universal a niños y adolescentes, sería la estrategia óptima para la eliminación y control de la enfermedad
Gripe
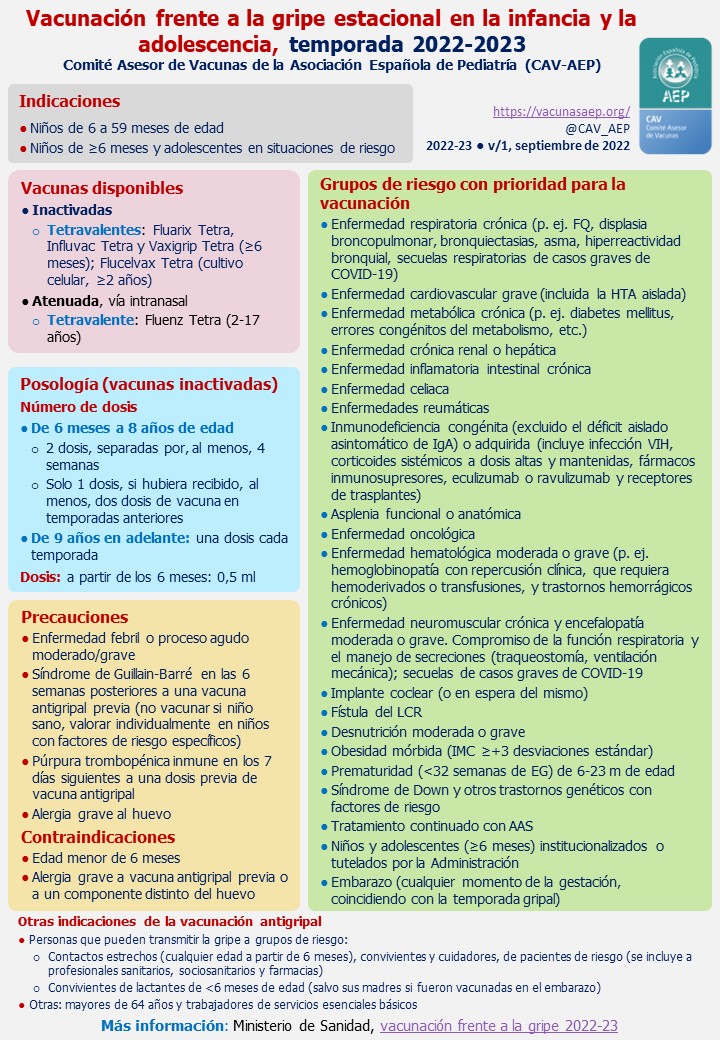
Al igual que ocurren en el caso del VHA, a pesar de que no existe una recomendación general para la vacunación frente a la gripe, son varios los grupos en los que está recomendada la vacunación tetravalente inactivada (solamente a partir de los 6 meses) por vía intramuscular o la atenuada (a partir de los 2 años de edad) por vía intranasal:
- Todos los niños entre 6 y 59 meses.
- Grupos de riesgo: niños mayores de 5 años o adolescentes con enfermedades de base que supongan un riesgo aumentado de padecer complicaciones (Ver Tabla I).
- Mayores de 5 años que convivan con pacientes de alto riesgo.
- Personas convivientes con niños menores de 6 meses.
- Profesionales sanitarios.
- Embarazadas, tanto para su protección como para el hijo futuro, en cualquier momento del embarazo.
Vacunación en situaciones especiales (incluyendo el embarazo), población de riesgo y viajeros
Existen recomendaciones específicas para aquellas mujeres que busquen una gestación, estén embarazadas o hayan dado a luz y estén lactando:
- Previo a la gestación: se debe comprobar y completar la vacunación propia de la edad.
- En caso de vacunas vivas inactivadas (TV, VVZ, fiebre amarilla, y fiebre tifoidea oral) se debe evitar la concepción durante las siguientes 4 semanas.
- Durante la gestación:
- Antigripal y de tipo mRNA de SARS-CoV2 en cualquier momento de la gestación.
- Tosferina (Tdpa): entre las semanas 27-36 (mejor 27-32) en cada embarazo.
- No existe recomendación para el uso de la vacuna frente al VPH.
- Contraindicación parar las vacunas vivas atenuadas: TV, VVZ, fiebre amarilla y fiebre tifoidea oral.
- Tras el embarazo y durante la lactancia
- Comprobar y completar las vacunas correspondientes a la edad.
- Fiebre amarilla: en lactantes menores de 9 meses se aconseja suspender la lactancia y extraer y desechar la leche durante 2 semanas.
- Tras la vacunación del VVZ, si aparecieran lesiones cutáneas, se debe evitar contacto con ellas.
- Capítulo 9. Profilaxis post-exposición.
- Capítulo 12. Inmigrante, refugiados y adoptados.
- Capítulo 14. Niños inmunodeprimidos o con tratamiento inmunosupresor.
- Capítulo 15. Niños con infección por VIH.
- Capítulo 16. Niños con trasplanta de progenitores hematopoyéticos y de órgano sólido.
- Capítulo 17. Niños con enfermedad crónica.
- Capítulo 18. Convivientes con pacientes con patología de riesgo.
- Es esencial aprovechar cualquier oportunidad para la información, educación y la vacunación individualizada del adolescente.
- Debemos completar el calendario de adolescentes no vacunados o incompletamente vacunados con las vacunas triple vírica, de la varicela o de la hepatitis B.
- No debemos olvidarnos de circunstancias especiales (embarazo, inmunodepresión, enfermedades crónicas, profilaxis post-exposición) y del adolescente viajero.
- Hidalgo Vicario MI, De Montalvo Jääskeläinen F, Martinón-Torres F, Moraga-LLop F, Cilleruelo Ortega MJ, Montesdeoca Melián A, et al. Calendario de vacunaciones del adolescente. Documento de Consenso. Madrid: Undergraf; 2021.
- Boletín Semanal en Red. Número 16. Año 2023. Centro Nacional de Epidemiología. ISCIII.
- Meningococcal vaccines: WHO position paper, November 2011. Wkly Epidemiol Rec. 2011 Nov 18;86(47):521-39. English, French. PMID: 22128384.
- Rosenstein NE, Perkins BA, Stephens DS, Popovic T, Hughes JM. Meningococcal disease. N Engl J Med. 2001 May 3;344(18):1378-88. doi: 10.1056/NEJM200105033441807. PMID: 11333996.
- European Centre for Disease Prevention and Control. Disease data from ECDC Surveillance Atlas for meningococcal disease. Fecha de acceso: sep 2020. Disponible en: https://ecdc.europa.eu/en/meningococcal-disease/surveillance-and-disease-data/atlas.
- Christensen H, May M, Bowen L, Hickman M, Trotter CL. Meningococcal carriage by age: a systematic review and meta-analysis. Lancet Infect Dis. 2010 Dec;10(12):853-61. doi: 10.1016/S1473-3099(10)70251-6. Epub 2010 Nov 11. Erratum in: Lancet Infect Dis. 2011 Aug;11(8):584. PMID: 21075057.
- Rivero-Calle I, Raguindin PF, Gómez-Rial J, Rodriguez-Tenreiro C, Martinón-Torres F. Meningococcal Group B Vaccine For The Prevention Of Invasive Meningococcal Disease Caused By Neisseria meningitidis Serogroup B. Infect Drug Resist. 2019 Oct 9;12:3169-3188. doi: 10.2147/IDR.S159952. PMID: 31632103; PMCID: PMC6793463.
- Martinón-Torres F, Banzhoff A, Azzari C, De Wals P, Marlow R, Marshall H, et al. Recent advances in meningococcal B disease prevention: real-world evidence from 4CMenB vaccination. J Infect. 2021 Jul;83(1):17-26. doi: 10.1016/j.jinf.2021.04.031. Epub 2021 Apr 30. PMID: 33933528.
- Castilla J, García Cenoz M, Abad R, Sánchez-Cambronero L, Lorusso N, Izquierdo C, et al. Effectiveness of a Meningococcal Group B Vaccine (4CMenB) in Children. N Engl J Med. 2023 Feb 2;388(5):427-438. doi: 10.1056/NEJMoa2206433. PMID: 36724329.
- Martinón-Torres F, Taha MK, Knuf M, Abbing-Karahagopian V, Pellegrini M, Bekkat-Berkani R, et al. Evolving strategies for meningococcal vaccination in Europe: Overview and key determinants for current and future considerations. Pathog Glob Health. 2022 Mar;116(2):85-98. doi: 10.1080/20477724.2021.1972663. Epub 2021 Sep 27. PMID: 34569453; PMCID: PMC8933022.
- Abara, WE, Bernstein KT , Lewis FMT, Schillingerv JA, Feemster K , Pathela P, et al. Effectiveness of a serogroup B outer membrane vesicle meningococcal vaccine against gonorrhoea: a retrospective observational study. The Lancet Infectious Diseases. 2022.
- Bruxvoort KJ, Lewnard JA, Chen LH, Tseng HF, Chang J, Veltman J, et al. Prevention of Neisseria gonorrhoeae With Meningococcal B Vaccine: A Matched Cohort Study in Southern California, Clinical Infectious Diseases, 2022; ciac436.
- Comité Asesor de Vacunas (CAV-AEP). Manual de Inmunizaciones en línea de la AEP. Capítulo 42. [Internet]. Madrid: AEP; 2023. Disponible en: https://vacunasaep.org/documentos/manual/cap-42.
- Situación de COVID-19 en España a 26 de enero de 2022. Equipo COVID-19. RENAVE. CNE. CNM (ISCIII).
- Comité Asesor de Vacunas (CAV-AEP). Manual de Inmunizaciones en línea de la AEP [Internet]. Madrid: AEP; 2023. Disponible en: http://vacunasaep.org/documentos/manual/manual-de-vacunas.
- https://www.sanidad.gob.es/profesionales/saludPublica/ccayes/alertasActual/nCov/documentos/Informe_GIV_comunicacion_20220131.pdf.
- SAGE Working Group. Report on pertussis vaccines. www.who.int/immunization/sage/meetings/2015/april/1_Pertussis_report_final.pdf.
- Martinón-Torres F, Heininger U, Thomson A, Wirsing von König CH. Controlling pertussis: how can we do it? A focus on immunization. Expert Rev Vaccines. 2018 Apr;17(4):289-297. doi: 10.1080/14760584.2018.1445530. Epub 2018 Mar 12. PMID: 29482390.
- Hidalgo Vicario MI, De Montalvo Jääskeläinen F, Martinón-Torres F, Moraga-LLop F, Cilleruelo Ortega MJ, Montesdeoca Melián A, et al. Calendario de vacunaciones del adolescente. Documento de Consenso. Madrid: Undergraf; 2021.
- Rivero-Calle I, Raguindin PF, Gómez-Rial J, Rodriguez-Tenreiro C, Martinón-Torres F. Meningococcal Group B Vaccine For The Prevention Of Invasive Meningococcal Disease Caused By Neisseria meningitidis Serogroup B. Infect Drug Resist. 2019 Oct 9;12:3169-3188. doi: 10.2147/IDR.S159952. PMID: 31632103; PMCID: PMC6793463..
- Martinón-Torres F, Banzhoff A, Azzari C, De Wals P, Marlow R, Marshall H, Pizza M, Rappuoli R, Bekkat-Berkani R. Recent advances in meningococcal B disease prevention: real-world evidence from 4CMenB vaccination. J Infect. 2021 Jul;83(1):17-26. doi: 10.1016/j.jinf.2021.04.031. Epub 2021 Apr 30. PMID: 33933528.
- Martinón-Torres F, Taha MK, Knuf M, Abbing-Karahagopian V, Pellegrini M, Bekkat-Berkani R, et al. Evolving strategies for meningococcal vaccination in Europe: Overview and key determinants for current and future considerations. Pathog Glob Health. 2022 Mar;116(2):85-98. doi: 10.1080/20477724.2021.1972663. Epub 2021 Sep 27. PMID: 34569453; PMCID: PMC8933022.
- Comité Asesor de Vacunas (CAV-AEP). Manual de Inmunizaciones en línea de la AEP [Internet]. Madrid: AEP; 2023. Disponible en: http://vacunasaep.org/documentos/manual/manual-de-vacunas.
Vacunación durante la gestación: antigripal, de tipo mRNA de SARS-CoV2 en cualquier momento de la gestación, y tosferina (Tdpa): entre las semanas 27-36 (mejor 27-32) en cada embarazo
Para la inmunización en circunstancias especiales se puede visitar la página del CAV de la AEP (https://vacunasaep.org/documentos/ manual/seccion-iii)
Dado lo extenso y específico del tema en cuestión dejamos a su disposición el enlace a la página web para inmunización en circunstancias especiales (https://vacunasaep.org/documentos/manual/seccion-iii) donde podrán encontrar indicaciones para los siguientes casos que pueden ser de interés en el caso de los pacientes adolescentes:
De entre ellos, se resalta la necesidad de re-vacunación del paciente oncológico y la pauta de vacunación acelerada en niños y adolescentes con vacunación inadecuada que incluye Hepatitis B (3 dosis), VVZ (2 dosis) y TV (2 dosis); y que se trata de forma más extensa en el Capítulo 11.
Los niños viajeros deberían ser derivados al centro de vacunación internacional (idealmente al menos 4 semanas antes del viaje)
Por otro lado, cabe destacar que los niños viajeros deberían ser derivados al centro de vacunación internacional (idealmente al menos 4 semanas antes del mismo), y cuyas indicaciones se desarrollan con detalle en el Capítulo 13.
Conclusiones
Conflictos de interés (Rivero Calle, Irene)
He recibido honorarios por conferencias de MSD, GSK, Sanofi y Pfizer.
He recibido becas/ayudas de investigación de Sanofi Pasteur, MSD, Novartis y Pfizer.
He recibido honorarios por consultorías para Pfizer, MSD, Sanofi.
He participado como subinvestigador en ensayos clínicos de vacunas de Ablynx, Abbot, Seqirus, Sanofi Pasteur MSD, Sanofi Pasteur, Cubist, Wyeth, Merck, Pfizer, Roche, Regeneron, Jansen, Medimmune, Novavax, Novartis y GSK.
Pertenezco a la JD del CAV-AEP.
Tablas y figuras
Tabla I. Recomendaciones del CAV-AEP para la vacunación antigripal en la infancia y la adolescencia 2022-2023
Figura 1. Calendario común de vacunación a lo largo de toda la vida 2023 del Consejo Interterritorial
Disponible en: https://www.sanidad.gob.es/areas/promocionPrevencion/vacunaciones/calendario-y-coberturas/docs/CalendarioVacunacion_Todalavida.pdf.
Figura 2. Calendario de inmunizaciones de la Asociación Española de Pediatría (CAV_AEP) 2023
Disponible en: https://vacunasaep.org/profesionales/calendario-de-inmunizaciones-de-la-aep-2023.
Figura 3. Propuesta de esquema de vacunación frente a tosferina completo desde el lactante al adolescente y adultos
Extraído de Martinon-Torres et al. Exp Vacc Rev 2018.
Bibliografía
Bibliografía recomendada