Protocolo – Guía clínica del dolor abdominal funcional
Guía clínica del dolor abdominal funcional
J.M Marugán de Miguelsanz(1,2), C. Alonso Vicente(1), P. Alonso López(1).
(1)Sección de gastroenterología y nutrición pediátrica. Hospital Clínico Universitario de Valladolid.(2)Profesor Titular de Pediatría. Facultad de Medicina de Valladolid.
Fecha de recepción: 11-01-2021
Fecha de publicación: 28-02-2021
Adolescere 2021; IX (1): 76-85
Resumen
|
El dolor abdominal recurrente (DAR) es uno de los motivos de consulta de carácter crónico más frecuente en pediatría. Solo encontramos causa orgánica en alrededor del 10% de los casos, tratándose la mayor parte de las veces de un trastorno funcional. En los nuevos criterios Roma IV se distinguen dentro de este último grupo 4 formas clínicas: dispepsia funcional, intestino irritable, migraña abdominal, y dolor abdominal no especificado. En su estudio inicial con frecuencia se recurre a exámenes sencillos de primer nivel diagnóstico, si bien se puede hablar de DAR funcional sin la realización de exámenes complementarios, con clínica compatible con dolor funcional, exploración física y crecimiento normal, y ausencia de luces rojas o signos de alarma. Se revisa el tratamiento del mismo, no existiendo evidencia de eficacia de ningún tratamiento farmacológico o dietético. Palabras clave: Dolor abdominal recurrente; Dolor abdominal funcional; Niño y adolescente. |
Abstract
|
Recurrent abdominal pain (RAP) is one of the most frequent chronic reasons for consultation in pediatrics. We will only find an organic cause in about 10 % of cases, being the majority a functional disorder. 4 clinical forms are distinguished within the latter group in the new Rome IV criteria: functional dyspepsia, irritable bowel syndrome, abdominal migraine, and functional abdominal pain not otherwise specified. Simple first-level diagnostic tests are often used in the initial study, although it is possible to speak of functional RAP without performing complementary tests if there is a compatible clinical picture, physical examination, normal growth, and absence of red lights. Its treatment is reviewed, and there is no evidence of efficacy of any pharmacological or dietary treatment. Key words: Recurrent abdominal pain; Functional abdominal pain; Child and adolescent. |
Introducción
El dolor abdominal recurrente (DAR) es un problema muy común, y uno de los motivos más frecuentes de consulta por patología crónica en Pediatría. Se estima que puede afectar a un 10% de niños y adolescentes en algún momento de su vida (4-25% según series)(1). Predomina en niñas hasta la pubertad (OR para sexo femenino 1,5)(2), pero después la frecuencia se iguala. Dicho dolor interfiere con las actividades diarias del sujeto, suele provocar pérdida de días de colegio, visitas a urgencias, a veces incluso hospitalizaciones o intervenciones quirúrgicas, e impacto económico(1), y la calidad de vida de estos pacientes suele ser peor que la de la población general3). Además, puede causar significativa ansiedad en padres y cuidadores, que se sienten sobrepasados por el temor a una enfermedad grave, e impotentes por ser incapaces de aliviar o mejorar los síntomas de su hijo.
El dolor abdominal recurrente (DAR) es uno de los motivos más frecuentes de consulta por patología crónica en Pediatría
Aunque como veremos a continuación, en su gran mayoría no entraña gravedad ni existe una causa orgánica subyacente, hay que resaltar la incertidumbre del médico que debe enfrentarse a la consulta reiterada por este motivo, ante la posibilidad de no estar realizando todas las pruebas complementarias necesarias para llegar a un diagnóstico correcto, dada la escasa especificidad clínica habitual del cuadro. Esta revisión trata de hacer comprender mejor esta entidad, para intentar ayudar en su manejo en la práctica clínica diaria.
Concepto
El concepto clásico de DAR descrito por Apley y Naish en 1958, y utilizado durante décadas, exigía la presencia de tres o más episodios de dolor abdominal, suficientemente intensos como para interferir la actividad normal del niño, en un periodo superior a 3 meses4). Se pretendía así diferenciarlo de multitud de cuadros agudos y transitorios causantes de dolor abdominal. Los autores hicieron esta descripción, sin ayuda de test diagnósticos, en una serie de 1000 escolares británicos, de los cuales el 10,8% referían padecer DAR, pensando en una única y bastante homogénea entidad que según ellos representaba un trastorno psicosomático en niños que eran con frecuencia muy nerviosos, exigentes, tímidos, ansiosos, y demasiado concienzudos. Posteriormente, se vio que el DAR no era una entidad única, sino que podía tener una variedad de causas incluyendo patología orgánica y trastornos funcionales.
Por lo tanto, esa definición inicial dio paso a los más consensuados criterios de Roma de trastornos funcionales gastrointestinales, aunque no refiriéndose al concepto global de Apley que comprendía todos los casos de DAR, incluso los orgánicos, sino solo a esa mayoría de formas funcionales del mismo. Los primeros que incluyeron criterios pediátricos fueron los criterios Roma II en 1999, tras la primera edición de los mismos en 1990, solo para adultos.
Los últimos publicados han sido los criterios Roma IV en 20165), valorando la evidencia científica actual, y ante la ausencia de datos científicos, mediante la experiencia clínica y el consenso entre el grupo de expertos. La época en que el diagnóstico de trastornos funcionales digestivos se hacía solo cuando se hubiera excluido una enfermedad orgánica, ha pasado ya, y ahora el clínico puede llevar a cabo un diagnóstico positivo de trastorno funcional sin pruebas que lo apoyen.
Según estos criterios Roma IV, el dolor abdominal funcional se incluye en los trastornos funcionales gastrointestinales en niños mayores de 4 años (niños y adolescentes), y se refiere a aquellos cuadros sin etiología conocida tras una apropiada evaluación, y no explicados por anomalías estructurales o bioquímicas, con una duración de al menos 2 meses, y que interfieran de manera importante en la calidad de vida del niño y su familia.
Según los recientes criterios Roma IV, hablamos de dolor abdominal funcional en aquellos cuadros sin etiología conocida tras una apropiada evaluación, y no explicados por anomalías estructurales o bioquímicas, con una duración de al menos 2 meses, y que interfieran de manera importante en la calidad de vida del niño y su familia
Etiopatogenia
En más del 90% de los casos no seremos capaces de encontrar una causa orgánica para el mismo, si bien situaciones tan frecuentes como el estreñimiento funcional o la intolerancia a la lactosa tardía tipo adulto, están en la base de muchos de estos cuadros sin un diagnóstico preciso de origen orgánico, y su tratamiento en estos casos puede mejorar o hacer desaparecer el cuadro.
Aunque infrecuente, el DAR de causa orgánica puede tener una cantidad innumerable de causas. Sin embargo, con mucha diferencia el más frecuente es el dolor funcional, que supone al menos el 90% de los casos
Aunque infrecuente, el DAR de causa orgánica puede tener una cantidad innumerable de causas, no solo digestivas, sino también urinarias, genitales en niñas y adolescentes, sobre todo durante la pubertad, o incluso motivos generales o sistémicos muy diversos. A título de recordatorio, mostramos a continuación solo algunas de las más frecuentes6):
Gastrointestinales
Hernias, duplicaciones, divertículo de Meckel, reflujo gastroesofágico, esofagitis eosinofílica, gastritis crónica, ulcus, patología biliar, pancreatitis, fibrosis quística, celiaca, enfermedad inflamatoria intestinal crónica, linfadenitis mesentérica, alergia alimentaria, poliposis, estreñimiento, parasitosis, malabsorción de lactosa, bridas.
Urinarias
Litiasis, hipercalciuria, infecciones, hidronefrosis, reflujo vesicoureteral, u otras anomalías urológicas.
Genitales femeninas
Hematocolpos, quiste de ovario, torsión de ovario, vulvovaginitis, anexitis, dismenorrea, tumores.
Generales
Hiperlipemia, hiperparatiroidismo, diabetes, porfirias, drepanocitosis, tuberculosis, brucelosis, fiebre tifoidea, intoxicación crónica por plomo, linfoma, tumor carcinoide, fármacos, enfermedades periódicas, migraña, síndrome de la costilla deslizante, etc.
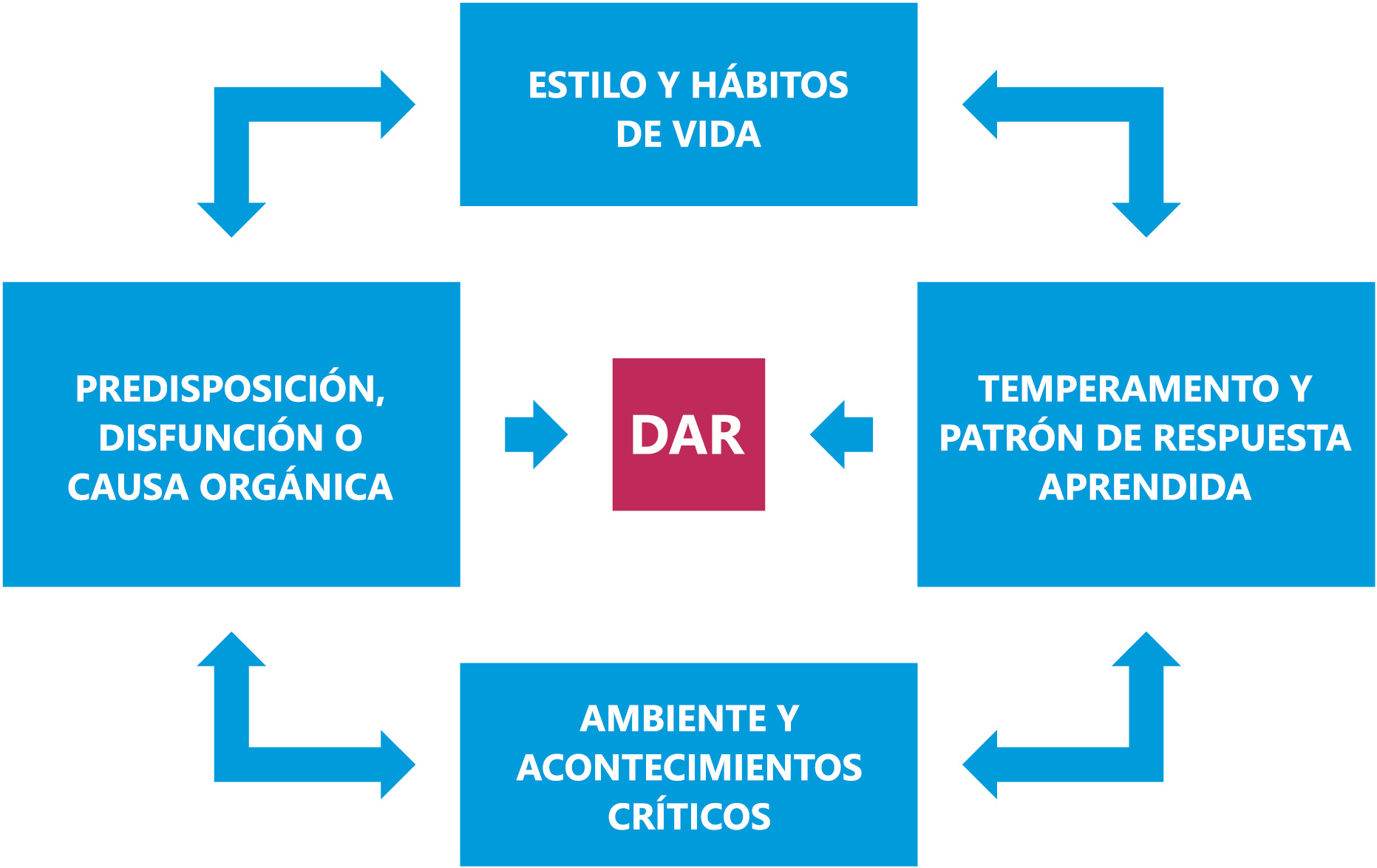
Sin embargo, con mucha diferencia el más frecuente es el dolor funcional. Su fisiopatología no está ni mucho menos clara. La explicación al dolor y a su mecanismo de producción más aceptado radica en el modelo clásico multifactorial de Levine y Rappaport7). Según esta propuesta, el DAR sería el resultado de la interacción de una serie de factores primarios (Figura 1): predisposición, disfunción o trastorno orgánico por un lado, con determinados estilos y hábitos de vida, temperamento y patrones de respuesta aprendidos, y finalmente la presencia de un ambiente y acontecimientos críticos. Ante esta conjunción de hechos, y ante un mismo factor predisponente, disfunción o causa orgánica, puede ocurrir que un paciente esté asintomático, y otro por el contrario refiera intenso dolor abdominal recurrente.
Posteriormente, Hyams y col. acuñaron el modelo biopsicosocial para el mismo8). La enfermedad surgiría de una combinación de enfermedad orgánica, trastorno funcional, trastorno somatomorfo, una relación alterada entre el paciente y la sociedad, y una particular interpretación de los síntomas y
reacciones familiares.
Se ha especulado finalmente que los niños con DAR podrían tener un probable trastorno de motilidad o bien una hipersensibilidad visceral, con alteraciones en el eje intestino-cerebro y en las relaciones entre el sistema nervioso central y el sistema nervioso autónomo intestinal, posiblemente debidas a las complejas interacciones entre el ambiente y factores hereditarios1,6,9,10). Sin embargo, los estudios en este sentido son de escasa aplicación práctica.
Una proporción de pacientes con DAR funcional desarrollan posteriormente otros trastornos funcionales como el síndrome de intestino irritable o la migraña, sobre todo si hay factores que favorezcan su persistencia, como disfunciones familiares, comorbilidades, o conductas familiares que lo refuercen(11).
Clínica
DAR funcional
Hay una serie de características clínicas generales más propias del dolor funcional. Su presencia apoyará esa posibilidad, frente a un dolor de causa orgánica. Si el dolor es periumbilical, difuso o el niño no describe sus características, si nunca es nocturno, es de duración breve y resolución espontánea, y no tiene relación con la ingesta ni el ejercicio, se incrementan las posibilidades de tener un carácter funcional. Asimismo, en el DAR funcional no suele haber síntomas acompañantes, salvo los vegetativos asociados al dolor, ni afectación del estado general ni nutricional. En el ambiente del niño hay frecuentes factores de estrés ambiental, y suele haber antecedentes familiares de dolor crónico o trastornos funcionales, como el intestino irritable o la migraña.
Sin embargo, también dentro del DAR funcional han tratado de distinguirse diferentes cuadros, con una sintomatología propia. En los trastornos con dolor abdominal funcional (H2) definidos en los criterios Roma IV5), se distingue entre:
-
El dolor funcional tiene unas características propias, aunque dentro del mismo se distinguen hoy 4 tipos: dispepsia funcional, síndrome de intestino irritable, migraña abdominal, y dolor abdominal funcional sin otra etiología especificada
H2 a. Dispepsia funcional
- H2 b. Síndrome de intestino irritable
- H2 c. Migraña abdominal
- H2 d. Dolor abdominal funcional sin otra etiología especificada
Solo en algunas ocasiones conseguiremos recoger en la historia clínica características que nos permitan encuadrar el DAR funcional en uno u otro tipo de los descritos. En la Tabla II podemos ver resumidos sus criterios diagnósticos Roma IV, y las principales características de los mismos:
- Sugerirá una dispepsia funcional, la aparición de síntomas en la parte alta del abdomen, sobre todo en la región epigástrica, sin relación con la deposición, pero sí generalmente con la ingesta.
- El síndrome de intestino irritable se manifestará sobre todo con síntomas más bien en la parte baja del abdomen, y sobre todo con cambios en las heces, o alivio con la deposición, alternancia diarrea/estreñimiento, meteorismo o sensación de evacuación incompleta. Es la forma más común de dolor funcional en el mundo desarrollado, suponiendo en algún caso más del 50% de los casos de DAR12).
- La migraña abdominal es típicamente episódica, con síntomas asociados, y con largos periodos intercríticos normales, aunque no siempre aparece cefalea en los primeros años.
- Finalmente, en muchas ocasiones el niño no nos dará suficiente información sobre el cuadro, y tendremos que encuadrarlo dentro del dolor abdominal funcional no especificado, al no tener criterios suficientes para encuadrarlo en alguno de los otros tres tipos.
Todos ellos exigen la presencia de dolor al menos 4 días al mes, excepto la migraña abdominal.
DAR orgánico. Signos de alarma
Por el contrario, la presencia de “luces rojas” o signos de alarma deberían ponernos más sobre la pista de un dolor de causa orgánica2,6,9). Los signos, de este tipo más importantes quedan resumidos a continuación:
La presencia de “luces rojas” o signos de alarma deberían ponernos más sobre la pista de un dolor de causa orgánica
- Dolor no periumbilical, bien localizado, o irradiado, sobre todo en cuadrantes inferior y superior derechos.
- Dolor o diarrea que le despierta por la noche.
- Pérdida de peso involuntaria, talla estacionada, retraso puberal.
- Síntomas asociados: Anorexia, vómitos persistentes, pirosis, diarrea crónica, sindrome miccional, infecciones urinarias, disfagia, odinofagia, artralgias/artritis.
- Signos asociados y datos de laboratorio: ictericia, fiebre inexplicada, masa abdominal palpable, visceromegalias, lesiones perianales, anemia, VSG alta.
- Hemorragia digestiva: visible, o bien presencia de sangre oculta en heces.
- Antecedentes familiares: Gastritis crónica y ulcus, Helicobacter pylori, enfermedad inflamatoria intestinal crónica, celiaca, litiasis renal, etc.
Hay insuficiente evidencia para establecer que la naturaleza del dolor o la presencia de muchos de estos síntomas asociados, así como la presencia de ansiedad, depresión, problemas conductales o eventos vitales recientes negativos en la familia, o ciertas luces rojas, puedan discriminar entre orgánico y funcional(3,13). Sin embargo, suelen ser de utilidad práctica en la clínica diaria.
No vamos a entrar en describir las características clínicas específicas de muchas causas de dolor abdominal recurrente, que deberían orientarnos hacia una causa orgánica concreta, aunque algunas están ya recogidas entre los signos de alarma mencionados.
Diagnóstico
Como todo estudio en medicina, el análisis del DAR precisará de una cuidadosa historia clínica, y una completa exploración física, con valoración por supuesto del crecimiento y estado nutricional del paciente. En el caso del estreñimiento funcional, sobre todo cuando este no es el principal motivo de consulta pero puede existir una retención fecal crónica, o bien los padres desconocen el hábito intestinal del niño, el tacto rectal será preceptivo y nos ayudará a comprobar la presencia constante de heces en la ampolla rectal. Este hallazgo debe animarnos a su tratamiento, para comprobar si la regularización del hábito intestinal provoca la mejoría o incluso desaparición del dolor.
El análisis del DAR precisará de una cuidadosa historia clínica, y una completa exploración física, con valoración del crecimiento y estado nutricional del paciente
En cuanto a las exploraciones complementarias en el DAR, su número podría ser interminable si no lo dirigimos adecuadamente, debido a las innumerables, aunque infrecuentes, causas de DAR de posible causa orgánica.
Primer nivel de estudio del DAR
Para facilitar el manejo del cuadro, se ha establecido clásicamente un primer nivel de estudio del DAR, cuando no hay un diagnóstico claro en la primera evaluación, con una serie de técnicas básicas que puedan ayudar en su manejo. No existe evidencia alguna de su utilidad en ausencia de signos de alarma, y no son imprescindibles en la mayoría de casos de DAR funcional, pero se recurre a ellas con frecuencia ante la reiteración de consultas. En ocasiones su realización tranquiliza al médico que los realiza y alivia la ansiedad de la propia familia, y no son especialmente cruentas ni costosas. Sin ánimo de ser dogmático, para los padres suele ser más sencillo entender que pueda tratarse de un trastorno funcional cuando según ellos ya le han realizado “las pruebas” a su hijo. Recurrir a la segunda opinión de un profesional con más experiencia en la materia ante casos de mala evolución, suele tener un efecto similar.
Debería incluirse en este nivel una analítica básica de sangre (hemograma, VSG y bioquímica completa) y de orina, y unos parásitos en heces (Tabla I). Seguramente debamos introducir también la serología de enfermedad celiaca, por su elevada prevalencia (1% de la población), y porque además en tres cuartas partes de los casos la celiaca se manifiesta con formas oligosintomáticas, como puede ser el DAR. Finalmente, podemos llevar a cabo una ecografía abdominal, que, aunque tiene un escaso rendimiento diagnóstico (hallazgos en el 10% en niños con signos sugerentes de organicidad, versus 1% en el resto)14), es una técnica incruenta y frecuentemente realizada en este primer nivel de estudio.
En los últimos años el estudio de parásitos en heces ha quedado reducido en algunos laboratorios de microbiología, a la determinación por técnicas rápidas de dos de los patógenos más relevantes en nuestro medio desde el punto de vista terapeútico, ambos protozoos, Crypstosporidium spp. y Giardia lamblia, generalmente por inmunocromatografía. Hay que tener en cuenta a la hora de poder descartar completamente una causa parasitaria, que la técnica microscópica clásica de huevos, quistes y parásitos, con o sin concentración de la muestra, no suele realizarse de rutina en esos centros, perdiendo muchas veces una información importante sobre helmintos y otros protozoos, posibles causantes de DAR.
No tan aceptadas en este primer nivel de estudio del DAR, podemos situar también otras pruebas sencillas y fácilmente a nuestro alcance, como el índice calcio/creatinina en micción aislada, para descartar una hipercalciuria idiopática, o la determinación de sangre oculta en heces, ya que un positivo en esta última podría ser una señal de alarma en la valoración de estos pacientes. Antiguamente esta última técnica era farragosa por su preparación y por el elevado número de falsos positivos, pero los test inmunoquímicos actuales no precisan de una preparación ni de una dieta especial previa, y en general es suficiente con recoger una sola muestra.
Finalmente, un test clínico de supresión de lactosa puede ayudar a descartar la frecuente existencia de una intolerancia a la lactosa forma genética tardía o tipo adulto (1 de cada 5-6 adultos en nuestro medio), conduciendo en ese caso a la resolución de los síntomas. Con la pérdida progresiva de la actividad lactasa, la sintomatología suele comenzar después de la primera infancia, cuando la ingesta de lactosa empieza a ser superior a su decreciente capacidad de digestión. Posteriormente debería llevarnos a comprobar su carácter primario o secundario (no olvidar que la malabsorción de lactosa es un hecho constante y secundario a la patología de la mucosa intestinal, como la observada en la enfermedad celiaca, la enfermedad inflamatoria intestinal crónica, parasitosis, enteropatía autoinmune, o atrofia intestinal en la malnutrición crónica, entre otras situaciones). También deberemos comprobar entonces si tiene un carácter frecuentemente transitorio tras una enteropatía aguda, en el contexto de un síndrome postenteritis, probando su reintroducción pasadas al menos 2-4 semanas.
Los test incruentos para el diagnóstico de infección por Helicobacter pylori (antígeno en heces o test del aliento) no están indicados en el dolor abdominal recurrente de apariencia funcional, sin otros signos de alarma, al no aceptarse en la edad pediátrica la estrategia “test and treat” utilizada en el adulto. El tratamiento erradicador en niños con dolor abdominal solo está indicado ante la presencia de patología demostrada. Son muy pocos los casos en que la erradicación del Helicobacter pylori conduce a la resolución del dolor, y las resistencias son crecientes con la antibioterapia indiscriminada, especialmente a claritromicina y metronidazol. Por ello, en caso de signos o síntomas de alarma, el diagnóstico precisará una endoscopia digestiva alta, con comprobación no solo de su presencia y sensibilidad a antibióticos, sino de la existencia o no de patología concreta que pueda justificar el cuadro (gastritis, duodenitis crónica o ulcus péptico). El objetivo de la investigación será por lo tanto identificar la causa de los síntomas, más que la existencia o no de infección por H. pylori15).
Tampoco incluiríamos en este nivel de estudio, pruebas también sencillas, asequibles, y frecuentemente utilizadas, pero de escasa utilidad en este cuadro, como la realización de una calprotectina fecal, solo útil ante una posibilidad real de enfermedad inflamatoria intestinal crónica, el coprocultivo y el urocultivo.
Segundo nivel de estudio del DAR
Ante pruebas básicas o de primer nivel alteradas, clínica no típica de DAR funcional, o presencia de signos de alarma, tendremos que recurrir a otras técnicas complementarias en función de los hallazgos clínicos. La relación de exploraciones que podemos realizar para llegar a un diagnóstico puede ser interminable. A título de ejemplo mencionamos solo algunas, que probablemente deban llevarse a cabo en un segundo nivel asistencial, tras derivación al gastroenterólogo:
- Test de H2 espirado tras sobrecarga oral de azúcares
- Técnicas radiológicas digestivas o renales, o de medicina nuclear
- pH-metría esofágica
- Endoscopia digestiva alta y/o baja
- Pruebas alérgicas (alimentos)
- Niveles de plomo en sangre
- Catecolaminas y porfirinas en sangre y orina
- EEG
- Mantoux
- Test del sudor
- Laparoscopia exploradora
- Consulta especializada: Gastroenterología, Psiquiatría infantil
En una niña durante el desarrollo puberal, ante un dolor localizado en el punto anexial correspondiente, será preciso descartar también una causa ovárica, precisando un examen ginecológico y ecográfico.
Finalmente, ante un dolor persistente en FID, tras un episodio de sospecha inicial de apendicitis aguda no confirmada ni intervenida, sin otros síntomas asociados y negatividad de otros exámenes, una laparoscopia exploradora permite identificar con frecuencia causas apendiculares o periapendiculares para el dolor (sobre todo adherencias fibrosas, pero también cuerpos extraños, parásitos, pequeños tumores benignos, etc.), y la apendicectomía y liberación de posibles adherencias resuelven en muchas ocasiones el cuadro.
Sin embargo, en ausencia de luces rojas no suele haber necesidad de extensas pruebas complementarias(11).
En síntomas sugerentes de dispepsia funcional, el diagnóstico diferencial de patología orgánica con manifestaciones similares, debería incluir básicamente la patología digestiva alta más frecuente: enfermedad por reflujo gastroesofágico, esofagitis eosinofílica (sobre todo en alérgicos), gastritis crónica, úlcera péptica, enfermedad hepatobiliar, patología pancreática, etc.
En cambio, ante síntomas de dolor asociado a alteraciones en las heces o ritmo de las deposiciones, el síndrome de intestino irritable tendrá sobre todo que diferenciarse de la enfermedad inflamatoria intestinal crónica, de la celiaca, o del estreñimiento simple funcional.
La intolerancia a la lactosa no tiene en muchas ocasiones una clínica específica, debiendo estar presente en la sospecha diagnóstica ante cualquier tipo de dolor abdominal de apariencia funcional, sin repercusión nutricional.
Finalmente, según los criterios Roma IV de trastornos gastrointestinales funcionales en la infancia, podemos realizar un diagnóstico “positivo” de dolor abdominal funcional, incluso sin pruebas complementarias especiales ni complejas, si se dan las siguientes circunstancias:
Sin embargo, podemos realizar un diagnóstico “positivo” de dolor abdominal funcional, sin pruebas complementarias complejas, si se dan las siguientes circunstancias: historia clínica compatible, exploración física, crecimiento y desarrollo normales, exámenes complementarios de primer nivel normales, y ausencia de luces rojas o signos de alarma
- Historia clínica compatible
- Exploración física, crecimiento y desarrollo normales
- Exámenes complementarios de primer nivel normales
- Ausencia de luces rojas o signos de alarma
Tratamiento del dolor abdominal funcional
Una vez establecido el diagnóstico de DA funcional, su manejo también requiere unas pautas concretas, que bien aplicadas suelen conducir a la mejoría del cuadro.
En primer lugar, hay que tranquilizar a la familia y explicar el proceso diagnóstico, sobre todo desde una visión multifactorial o biopsicosocial. Es clave conseguir que los padres y el niño acepten la naturaleza funcional del dolor. Hay que hacerles ver que el cuadro no es amenazante para la vida, no existe una enfermedad subyacente severa, y que en dos tercios de los casos mejorará.
No es preciso establecer un diagnóstico en la primera consulta. El médico debe estar disponible para futuros contactos. Debemos pautar revisiones periódicas para reevaluar el caso, confirmar el diagnóstico y vigilar la aparición de posibles signos de alarma, que nos lleven a emprender nuevos estudios.
Las causas orgánicas graves antes o después se expresarán clínicamente.
Se debe evitar el etiquetado de “psicológico”, mejor utilizar el término “dolor abdominal funcional”.
Es importante explicar a la familia que el dolor no es simulado sino real
Debemos evitar el etiquetado de “psicológico”. Es mejor utilizar el término “dolor abdominal funcional”. Es importante hacer ver a la familia que el dolor no es simulado sino real, y que el niño ha tenido y seguramente tiene dolor la mayor parte de las ocasiones que lo manifiesta.
Es importante modificar los factores de estrés, su estilo de vida y las conductas que desencadenan el dolor o que refuerzan el comportamiento doloroso. Por otra parte, hay que fomentar las habilidades que aumentan la resiliencia o entereza para asumir y afrontar la realidad. La excesiva vigilancia parental para los síntomas puede empeorar el dolor.
Un punto clave es establecer un régimen de vida familiar y escolar normal. Debemos evitar el absentismo escolar prolongado, imponiendo una vuelta gradual al colegio, más que una vuelta brusca a un horario normal.
Se deben evitar los tratamientos farmacológicos, generalmente ineficaces y que sin embargo pueden reforzar el cuadro. Se han probado especialmente distintos antiespasmódicos, con resultados dispares, y la heterogeneidad de los estudios existentes no permite sacar conclusiones al respecto. La falta de evidencia de efectividad para cualquier droga sugiere que hay poca justificación para guiar decisiones de tratamiento, salvo su uso en ensayos clínicos1,16,17). Solo hay mínima evidencia de mejoría con probióticos, sobre todo en el intestino irritable, y únicamente a corto plazo, aunque es insuficiente para aconsejar una cepa determinada en cualquier guía de práctica clínica, y la evidencia es limitada sobre el mantenimiento de esa mejoría varios meses tras el tratamiento1,2,3,12,18).
Pero la mejor evidencia de eficacia viene dada por terapias psicológicas. Así, y también a corto plazo, han demostrado eficacia la terapia congnitivo-conductal, técnicas de distracción, y la hipnoterapia2,11,19).
No hay evidencia de eficacia en el tratamiento para distintos fármacos y modificaciones dietéticas, salvo en algún caso para terapias psicológicas
En general hay que evitar cambios dietéticos20). No se ha demostrado la eficacia de una modificación de la fibra dietética, salvo que coexista estreñimiento2). La alergia alimentaria como causa de DAR, y la sensibilidad al gluten no celiaca, son entidades infrecuentes en niños. Una dieta pobre en FODMAPS (Fermentable Oligo-saccharides, Di-saccharides, Mono-saccharides And Polyols), puede jugar un papel en el desencadenamiento del dolor en algunos pacientes con intestino irritable12), y se ha utilizado en los últimos años en distintos trastornos funcionales digestivos. En teoría una dieta baja en FODMAPS reduce la cantidad de carbohidratos de cadena corta dietéticos que podrían inducir producción de gas, distensión de intestino grueso, meteorismo y dolor abdominal11). No hay experiencia suficiente aún con estas dietas en niños9). Únicamente algunos enfermos con una ingesta excesiva de sorbitol y fructosa líquida, especialmente en alimentos manufacturados, se pueden beneficiar de una importante reducción de los mismos.
En todo caso, debemos valorar con cautela la respuesta positiva a cualquier tratamiento. El efecto placebo es muy frecuente en sintomatología digestiva11).
Finalmente, podemos hacer un uso apropiado de segundas opiniones, y valorar una interconsulta a gastroenterología pediátrica, donde se suele reafirmar su carácter funcional, favoreciendo la mejoría del cuadro, o bien en casos concretos, a psiquiatría infantil.
Tablas y figuras
Tabla I. Pruebas a valorar en el 1º nivel de estudio del DAR de causa no aclarada
|
Tabla II. Trastornos con dolor abdominal funcional. Roma IV
|
Dispepsia funcional (DF) |
Síndrome de intestino irritable (SII) |
Migraña abdominal (MA) |
DA funcional no especificado |
|
|
Al menos 2 episodios de:
|
|
Figura 1. Modelo multifactorial de DAR funcional de Levine y Rappaport(7)
Bibliografía
- Abbott RA, Martin AE, Newlove-Delgado TV, Bethel A, Whear RS, Thompson-Coon J, et al. Recurrent Abdominal Pain in Children: Summary Evidence From 3 Systematic Reviews of Treatment Effectiveness. J Pediatr Gastroenterol Nutr. 2018; 67(1): 23-33.
- Andrews ET, Beattie RM, Tighe MP. Functional abdominal pain: what clinicians need to know. Arch Dis Child. 2020; 105(10): 938-44.
- Di Lorenzo C, Colletti RB, Lehmann HP, Boyle JT, Gerson WT, Hyams JS, et al. AAP Subcommittee; NASPGHAN Committee on Chronic Abdominal Pain. Chronic Abdominal Pain In Children: a Technical Report of the American Academy of Pediatrics and the North American Society for Pediatric Gastroenterology, Hepatology and Nutrition. J Pediatr Gastroenterol Nutr. 2005; 40(3): 249-61.
- Apley J, Naish N. Recurrent abdominal pains: a field survey of 1.000 school children. Arch Dis Child. 1958; 33(168): 165-70.
- Hyams JS, Di Lorenzo C, Saps M, Shulman RJ, Staiano AM, van Tilburg M. Childhood Functional Gastrointestinal Disorders: Child/Adolescent. Gastroenterology. 2016; 150: 1456-68.
- McFerron BA, Waseem S. Chronic Recurrent Abdominal Pain. Pediatrics in Review 2012; 33 (11): 509-17.
- Levine MD, Rappaport LA. Recurrent abdominal pain in school children: the loneliness of the long-distance physician. Pediatr Clin North Am. 1984; 31(5): 969–91.
- Hyams JS, Hyman PE. Recurrent abdominal pain and the biopsychosocial model of medical practice. J Pediatr. 1998; 133: 473-8.
- Brown LK, Beattie RM, Tighe MP. Practical management of functional abdominal pain in children. Arch Dis Child. 2016; 101(7): 677-83.
- Sandhu BK, Paul SP. Irritable bowel syndrome in children: pathogenesis, diagnosis and evidence-based treatment. World J Gastroenterol. 2014; 20(20): 6013-23.
- Gómez-Suárez R. Difficulties in the Diagnosis and Management of Functional or Recurrent Abdominal Pain in Children. Pediatr Ann. 2016; 45(11): e388-e393.
- El-Matary W, Spray C, Sandhu B. Irritable bowel syndrome: the commonest cause of recurrent abdominal pain in children. Eur J Pediatr. 2004; 163: 584–8.
- Gijsbers CF, Benninga MA, Schweizer JJ, Kneepkens CM, Vergouwe Y, Büller HA. Validation of the Rome III criteria and alarm symptoms for recurrent abdominal pain in children. J Pediatr Gastroenterol Nutr. 2014; 58(6): 779-85.
- Reust CE, Williams A. Recurrent Abdominal Pain in Children. Am Fam Physician. 2018; 97(12): 785-93.
- Jones NL, Koletzko S, Goodman K, Bontems P, Cadranel S, Casswall T, et al. on behalf of ESPGHAN, NASPGHAN. Joint ESPGHAN/NASPGHAN guidelines for the Management of Helicobacter pylori in Children and Adolescents (Update 2016). J Pediatr Gastroenterol Nutr. 2017; 64: 991–1003.
- Martin AE, Newlove-Delgado TV, Abbott RA, Bethel A, Thompson-Coon J, Whear R, Logan S. Pharmacological interventions for recurrent abdominal pain in childhood. Cochrane Database Syst Rev. 2017; 3(3):CD010973.
- Brusaferro A, Farinelli E, Zenzeri L, Cozzali R, Esposito S. The Management of Paediatric Functional Abdominal Pain Disorders: Latest Evidence. Paediatr Drugs. 2018; 20(3): 235-247.
- Newlove-Delgado T, Abbott RZ, Martin AE. Probiotics for Children with Recurrent Abdominal Pain. JAMA Pediatr. 2019; 173(2): 183-184.
- Fisher E, Law E, Dudeney J, Eccleston C, Palermo TM. Psychological therapies (remotely delivered) for the management of chronic and recurrent pain in children and adolescents. Cochrane Database Syst Rev. 2019; 4(4):CD011118.
- Newlove-Delgado TV, Martin AE, Abbott RA, Bethel A, Thompson-Coon J, Whear R, Logan S. Dietary interventions for recurrent abdominal pain in childhood. Cochrane Database Syst Rev. 2017 Mar 23;3(3):CD010972.
Bibliografía recomendada
- Abbott RA, Martin AE, Newlove-Delgado TV, Bethel A, Whear RS, Thompson-Coon J, et al. Recurrent Abdominal Pain in Children: Summary Evidence From 3 Systematic Reviews of Treatment Effectiveness. J Pediatr Gastroenterol Nutr. 2018; 67(1): 23-33. Actualización de la evidencia disponible sobre la eficacia de diversas medidas terapéuticas en el DAR en niños.
- Brusaferro A, Farinelli E, Zenzeri L, Cozzali R, Esposito S. The Management of Paediatric Functional Abdominal Pain Disorders: Latest Evidence. Paediatr Drugs. 2018; 20(3): 235-247. Revisión de la evidencia del tratamiento del dolor abdominal funcional.
- Sandhu BK, Paul SP. Irritable bowel syndrome in children: pathogenesis, diagnosis and evidence-based treatment. World J Gastroenterol. 2014; 20(20): 6013-23. Interesante revisión de todos los aspectos del dolor funcional.
- Brown LK, Beattie RM, Tighe MP. Practical management of functional abdominal pain in children. Arch Dis Child. 2016; 101(7): 677-83. Guía práctica de manejo del dolor abdominal funcional en niños.




