Mesa redonda Miscelánea. Il dolore toracico: un sintomo da valorizzare nell ́adolescente
Il dolore toracico: un sintomo da valorizzare nell´adolescente
G. Raiola (*), M.C. (**), D. Salerno (***), M. Aloe (****), V. Talarico (****), S. Spagnolo (****), M. Barreca (*), M.N. Pullano (****). (*) SOC di Pediatria, A.O. Pugliese-Ciaccio, Catanzaro (**) SOC di Ematoncologia Pediatrica, A.O. Pugliese-Ciaccio, Catanzaro (***) SOC di Chirurgia Pediatrica, A.O. Pugliese-Ciaccio, Catanzaro (****) U.O. di Pediatria, Università Magna Graecia di Catanzaro
Adolescere 2014;II (2): 45-58
Riassunto
|
Nell’infanzia e nell’adolescenza, i dolori toracici sono relativamente comuni e auto- limitanti. A causa della stretta associazione tra dolore toracico, cardiopatie e morte improvvisa negli adulti questo sintomo è causa di notevole ansietà nei ragazzi, nei loro genitori e nei medici. Gli Autori prendono in esame le più frequenti cause di dolore toracico, la diagnostica e l’eventuale trattamento. Infine anche il dolore toracico dovuto ad abuso di sostanze (in particolare cocaina) e monossido di carbonio. La conoscenza della patologia, un’accurata anamnesi ed un attento esame obiettivo permetteranno di formulare una corretta diagnosi e di pianificare un’adeguata strategia d’intervento. L’articolo è corredato da alcuni casi clinici. Parole chiave: Dolore toracico, Adolescenti, Diagnosi, Trattamento. |
Abstract
|
In childhood and adolescence chest pain is relatively common and self-limiting. Because of the close association between chest pain, heart disease and sudden death in adults, this symptom is a cause of considerable anxiety in the child, parents and doctors. The authors examine the most frequent causes of chest pain, diagnosis and treatment options. Finally, also chest pain due to the abuse of substances (particularly cocaine) and carbon monoxide will be discussed. The knowledge of the disease, careful anamnesis and a thorough physical examination will be very important to make a proper diagnosis and plan the appropriate intervention strategy. This article includes some clinical cases. Keywords: Chest pain, Adolescents, Diagnosis, Treatment. |
Il dolore toracico nel bambino e nell’adolescente è uno dei più comuni motivi per i quali si consulta il pediatra o ci si reca impronto soccorso.
Generalmente non rappresenta un sintomo importante e di rado è indice di patologie a carico dell’apparato cardiaco e respiratorio (1). Tuttavia la stretta associazione, nei pazienti adulti, tra dolore toracico, cardiopatie e morte improvvisa è spesso causa di notevole allarmismo. Una buona conoscenza del problema, un’accurata anamnesi ed un attento esame obiettivo permetterà di formulare una diagnosi e di adottare la più consona strategia d’intervento.
Si presenta in egual misura in entrambi i sessi, con un’età media di presentazione di 13 anni; talvolta è ricorrente. Nella maggior parte dei casi l’obiettività clinica è negativa ed i dati di laboratorio e/o strumentali sono di scarso aiuto.
Un’accurata anamnesi riveste un ruolo di primaria importanza. In particolare, bisognerà: mettere a proprio agio il paziente facilitando la descrizione del dolore con parole proprie (“il mio cuore andava di corsa”, “era come se avessi nel torace un uccello che batteva le ali”, “avvertivo palpitazioni”); valutare la personalità del paziente e dei genitori e le interazioni familiari (per escludere cause psicologiche del dolore); indagare su eventuali malattie cardiache e morti improvvise per cause cardiache nella familiarità.
Cause e manifestazioni cliniche
Dolore toracico idiopatico (fitte precordiali)
È la più frequente causa di dolore toracico in età pediatrica (12-85%). La fitta dolorosa può manifestarsi a riposo o nel corso di una moderata attività fisica, può durare da qualche secondo a qualche minuto, è ben localizzata in un punto situato lungo il margine sternale di sinistra o in corrispondenza dell’itto della punta. Può essere esacerbato dalla respirazione profonda o da una pressione manuale esercitata sullo sterno o sulla gabbia toracica. Non sono presenti segni d’infiammazione (2). La causa è sconosciuta. Se dopo un’accurata anamnesi, un accurato esame obiettivo e l’eventuale esecuzione di esami strumentali e di laboratorio non sarà riscontrata alcuna causa che possa essere alla base della sintomatologia dolorosa, potrà essere posta diagnosi di dolore toracico idiopatico.
Disordini muscolo-scheletrici
Costocondrite
È una delle più frequenti cause di dolore toracico; spesso preceduta da un’infezione delle vie respiratorie superiori o da un’attività fisica intensa. È più frequentemente riscontrata nel sesso femminile.
La sintomatologia dolorosa generalmente si esacerba con i profondi atti respiratori e può durare da qualche secondo a qualche minuto. Tende ad essere monolaterale, prevalentemente a livello della IV-VI articolazione condrocostale. Non sono presenti segni d’infiammazione. Elemento essenziale per la diagnosi dicostocondrite è rappresentato dalla riproducibilità clinica del dolore mediante la palpazione o la mobilizzazione della parte interessata o del braccio e della spalla omolaterale. In molti pazienti il disturbo si autolimita, anche se nel corso dell’adolescenza si possono avere intermittenti esacerbazioni.
Sindrome di Tietze
La sindrome di Tietze è un’ infiammazione non suppurativa localizzata dell’articolazione costocondrale, costosternale o sternoclavicolare. Rara in età pediatrica si manifesta più frequentemente negli adolescenti e nei giovani adulti. Non vi è differenza di sesso. Deve essere differenziata dalla costocondrite e dalle neoplasie. Nella maggior parte dei casi l’origine è sconosciuta. In tempi recenti si è giunti a pensare che l’origine del disturbo sia attribuiblile ad infezioni delle vie aeree superiori con tosse eccessiva, così come a traumi minimi che possono passare inosservati. Il dolore può essere riprodotto palpando la parte interessata.
Sindrome da scivolamento
Rara in età pediatrica, è caratterizzata da dolore localizzato alla parte inferiore del torace o ai quadranti addominali superiori, causato dalla dislocazione dell’ottava, nona o decima costa che, non essendo unite direttamente allo sterno ma piuttosto collegate tra loro tramite un setto fibrocartilagineo, sono ipermobili e soggette a traumi, anche di minima entità.
Stiramenti, spasmi, affaticamenti muscolari
Strappi muscolari interessanti il grande e/o piccolo pettorale possono verificarsi in giovani atleti (ginnasti e sollevatori di pesi). Fratture da sforzo possono osservarsi in tennisti e vogatori. I nuotatori possono presentare dolori toracici secondari ad un lungo trattenimento del respiro durante uno sforzo fisico particolarmente intenso. In letteratura è stata rilevata una stretta relazione tra sollevamento dei pesi e dissecazione dell’aorta, quale conseguenza di un intenso sforzo isometrico (3).
Recentemente è stato descritto un caso di un giovane atleta di 12 anni che presentò un improvviso dolore al rachide e al torace mentre praticava nuoto (stile a farfalla). Sottoposto a TAC del torace si diagnosticò dissecazione dell’aorta toracica discendente e un massivo emotorace destro (Standford Tipo B). Fu quindi sottoposto ad intervento chirurgico ma, a causa di un danno multi organo, morì dopo cinque giorni.
L’esame istopatologico di un campione dell’aorta dissecata, non evidenziò degenerazioni della media o necrosi. L’anamnesi personale e familiare era negativa per malattie cardio- vascolari. Questo paziente aveva una struttura muscolare da adulto, ma il diametro del lume dell’aorta non era proporzionato, in quanto era di soli 11 mm. In questo giovane paziente, a quanto pare, il nuoto ha provocato una manovra di Valsava con un innalzamento della pressione arteriosa acuta e conseguente dissezione su base meccanica di un’aorta toracica sottosviluppata (4).
Gli altri fattori di rischio che predispongono a dissezione dell’aorta in età pediatrico-adolescenziale sono le anomalie cardiovascolari (sindrome di Turner, sindrome di Marfan e altre anomalie del tessuto connettivo), l’ipertensione, i traumi e il sollevamento di pesi.
Traumi toracici non penetranti (traumi diretti)
L’impegno di molti teenagers in attività sportive li espone ad accidentali traumi del torace (nel 2% dei soggetti in età pediatrica). Il trauma toracico può causare dolore localizzato, tumefazione ed iperemia nella zona interessata. Se al dolore si associano aritmia e brevi atti respiratori, dovrà essere presa in considerazione la contusione del miocardio e un emopericardio (2).
Xifodinia
Causata da ipersensibilità al dolore del processo xifoideo, è caratterizzata da dolore localizzato in questa sede che può essere aggravato da mangiare un pasto pesante, tosse e movimenti di flessione e rotazione. La causa del dolore è sconosciuta. La compressione digitale sull’apofisi xifoidea suscita dolore sordo
Malformazioni della colonna vertebrale
Uno stimolo doloroso, nato da un’irritazione primitiva di una radice dorsale, può essere riferito alla parete toracica, cosi come si verifica nel caso delle radicoliti.
Questa sintomatologia può insorgere in pazienti con cifosi di grado elevato (malattia di Scheuerman) (2). La cifosi viene determinata da caratteristiche deformazioni a cuneo delle vertebre toraciche.
La stessa patogenesi vale anche per lo schiacciamento dei corpi vertebrali, lesioni scheletriche di natura infiammatoria o neoplastica, compressione del midollo spinale (tumore, ascesso epidurale, collasso vertebrale).
Disordini respiratori
Asma, Asma da sforzo
Le cause sono d’attribuire alla presenza di: dispnea, iperpnea, iperespansione polmonare, tosse, stiramento della muscolatura toracica, ansia, tachipnea. Il dolore è secondario allo stiramento dei muscoli della parete toracica o dalla stimolazione dei nervi intratoracici.
Polmonite, Pneumotorace, Pleurite, Pneumomediastino, Embolia polmonare, Inalazione di corpi estranei
A rischio per pneumotorace sono i soggetti con asma, fibrosi cistica, inalazione di corpo estraneo e sindrome di Marfan (2). Generalmente insorge con dispnea e dolore toracico. Lo pneumomediastino spontaneo è una rara entità clinica che difficilmente può essere osservata in pazienti pediatrici (5). L’embolia polmonare si osserva raramente in età pediatrica, può causare dolore toracico associato a tosse, emottisi, dispnea e tachicardia (6).
Disordini gastrointestinali
Esofagite da reflusso gastro-esofageo
I disordini gastrointestinali rappresentano circa l’8% delle cause di dolore toracico in questa fascia d’età (2). La più comune causa intestinale di dolore toracico è il reflussogastro-esofageo con esofagite. Il dolore può non essere specifico e descritto come un bruciore retrosternale, che viene ad essere aggravato dall’aumento della pressione intraddominale, dalla posizione supina ed è correlato con l’assunzione di cibo.
Il trattamento di prima scelta è rappresentato dagli anti H2 e dagli inibitori della pompa pro- tonica.
Spasmi o stenosi esofagee
Di rara osservazione, oltre al dolore retrosternale è presente disfagia.
Corpi estranei in esofago
Dolore retrosternale, disfagia e odinofagia
Ingestione di sostanze caustiche
Spesso a scopo suicidario; è presente dolore retrosternale edisfagia.
Iperdistensione gastrica
Può essere causata da iperdistensione dello stomaco causata da iperventilazione, deglutizione frequente di saliva, introduzione eccessiva di liquidi ed aerofagia.
Occasionalmente pazienti con ulcera peptica, colelitiasi, epatite,ascesso subfrenico o pancreati-te, possono presentare dolore riferito al torace inferiore (in quanto le porzioni posteriori e laterali del diaframma sono innervate dai nervi intercostali. Il sistema d’innervazione della porzione centrale e di quella anteriore, invece, determina un fenomeno di sinalgia delle regioni della spalla e del collo (6).
Miscellanea
Drepanocitosi
Nella malattia drepanocitica le crisi vaso-occlusive possono causare dolore toracico. La conseguenza immediata della crisi vasoocclusiva, generalmente del microcircolo, è il dolore, che tende a diffondersi dando spesso la sensazione soggettiva di “fine imminente”.
Il paziente si presenta al pronto soccorso in preda a crisi d’ansia, tachicardico, febbrile, talvolta con nausea e vomito. Quando viene interessato il macrocircolo oltre al dolore, in genere localizzato, si instaura un danno d’organo grave (SNC, polmoni). Lecrisi vaso-occlusive interessano prevalentemente l’apparato scheletrico, ma sono anche colpiti i muscoli, il polmone, gli organiaddominali e il sistema nervoso.
Il dolore addominale viene spesso interpretato come appendicite, gli infarti polmonari come polmoniti; per tale motivo possono essere intrapresi iter diagnostico-terapeutici inadeguati ed a volte dannosi.
Di fronte ad un paziente con crisi falcemica, i provvedimenti terapeuticida attuare sono:
— farmaci analgesici
— idratazione
— profilassi antibiotica
— trasfusione o eritroferesi
— somministrazione di O2
— supporto psicologico.
Il sintomo dolore deve essere affrontato prontamente, con decisione e razionalità. La scelta del farmaco deve essere effettuata conoscendo la risposta individuale all’analgesico e valutando i possibili effetti collaterali. Ad esempio, l’impiego di morfinici dovrà essere preclusa in pazienti con infarto polmonare, in quanto questi farmaci possono causare depressione respiratoria. L’infusione e.v. continua di narcotici può dare risultati eccellenti in termini di sedazione della sintomatologia algica, ma richiede la collaborazione di uno specialista in terapia del dolore. Altri trattamenti da associare sono l’idratazione, l’antibioticoterapia e l’eventuale trasfusione o exanguino-trasfusione.
Cause mammarie nella femmina
Secondarie a: tensione mammaria, mastite, traumi, terapia estroprogestinica, neoplasie (rare). Raramente il dolore toracico è associato a dispnea. In questi casi deve far sospettare una embolia polmonare (6).
Cause mammarie nel maschio
Secondarie a ginecomastie e neoplasie (rare).
Pleurodinia (Malattia di Bornholm)
Può verificarsi a qualsiasi età, ma è più comune nei bambini. È generalmente causata da infezioni da virus Coxakie B ed Echovirus. L’inizio è brusco, con febbre, dolore intenso, talora intermittente, al torace o nella parte alta dell’addome. Si possono associare: iperestesia locale, tumefazione dei muscoli colpiti e respiro superficiale. All’ascoltazione del torace possono essere apprezzati degli incostanti sfregamenti pleurici (generalmente evidenti in concomitanza degli episodi dolorosi). Gli esami di laboratorio sono di scarsa utilità; la conta dei GB è variabile, ma è frequente una elevazione dei granulociti neutrofili. La VES può presentare valori normali o particolarmente elevati. L’RX del torace è per lo più negativo. Non sono frequenti le complicanze anche se sono descritte: pleurite fibrinosa, pericardite, orchite e meningite asettica. Generalmente il decorso ha una durata di 2-3 giorni (2).
Caso clinico (osservazione personale)
Riportiamo il caso di un pz di 12 anni giunto alla nostra osservazione per improvvisa comparsa dolore toracico intenso, accentuato dagli atti del respiro, e febbre (T 38.0°C). All’EO: Condizioni generali discrete. Lamentava dolore toracico trafittivo, accentuato dagli atti del respiro, dalla digitopressione e dai movimenti di torsione del tronco. All’auscultazione del torace respiro aspro diffuso. Restante obiettività clinica negativa. Gli esami ematochimici effettuati mostravano una lieve leucocitosi neutrofila (GB 9.500, 62.8%, LI 22%, MO 8.8%), negatività degli indici di flogosi, dell’autoimmunità e degli enzimi cardiaci. ECG ed ecocardiogramma nella norma. Nel sospetto di un dolore toracico di origine pleuropolmonare il pz veniva sottoposto a radiografia del torace che risultava sostanzialmente negativa, ad eccezione di una sfumata obliterazione del seno costofrenico di sx. Dato l’esordio acuto della sintomatologia, la sostanziale negatività degli esami laboratoristici e strumentali veniva posto il sospetto di Malattia di Bornhol e richiesta sierologia per Coxakie virus risultata positiva.
Le manifestazioni cliniche del paziente sono progressivamente migliorate nell’arco di pochi giorni: il dolore toracico è completamente scomparso dopo 2 giorni senza alcuna terapia, ad ulteriore conferma dell’andamento benigno della malattia.
Sindrome S.A.P.H.O.
La sindrome S.A.P.H.O., il cui acronimo indica Synovitis, Acne, Pustulosis, Hyperostosis, Os- teomyelitis, è caratterizzata dall’associazione, anche non simultanea, di manifestazioni cuta- nee ed osteoarticolari, tanto da essere anche definita SKIBO (Skin and Bone disease). La sin- drome può comparire a qualsiasi età, interessando prevalentemente il periodo che intercorre tra l’infanzia e l’adolescenza; è inoltre caratterizzata da fasi di remissione e riacutizzazione. I soggetti affetti presentano usualmente dolore, edema e limitazione funzionale a carico delle articolazioni coinvolte e lesioni cutanee che vanno dalla pustolosi palmo-plantare all’acne cong- lobata. Il processo osteitico coinvolge particolarmente le articolazioni sterno-clavicolari, costo- sternali e manubrio-sternali, pertanto il quadro clinico d’esordio è spesso caratterizzato dalla comparsa graduale di dolore toracico, inizialmente a carattere episodico, a cui si può associare tumefazione dell’articolazione sterno-clavicolare e manubrio-sternale; in fase iniziale il dolore può essere l’unico sintomo. Nei bambini frequentemente si presenta con dolore acuto o cronico alle estremità, debilitante, caratterizzato da riacutizzazioni durante la notte ed interessamento delle ossa lunghe, accompagnato a febbre. Le principali manifestazioni cutanee sono l’acne conglobata e la pustolosi. L’acne conglobata è una variante suppurativa dell’acne volgare, carat- terizzata da formazioni ascessuali profonde e da cicatrici. Le sedi più frequentemente coinvolte sono il volto, il collo, la parte superiore del torace e il dorso. La diagnosi è essenzialmente clinica poiché la sindrome S.A.P.H.O. non possiede markers istologici, sierologici o radiologici tali da consentire di porre diagnosi di certezza (7,8).
Caso clinico (osservazione personale)
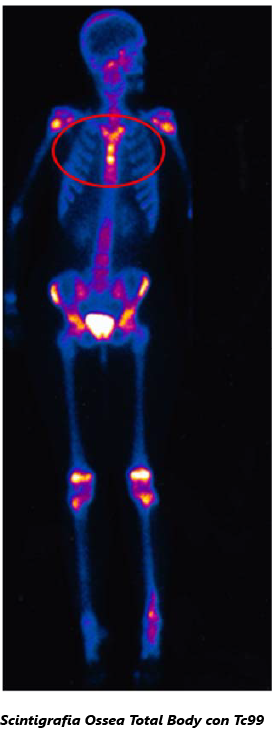
Riportiamo il caso clinico di una paziente di 12 anni giunta alla nostra osservazione per acne diffusa, progressivamente peggiorata nell’arco di poche settimane, e presenza di lesioni pustolose agli arti inferiori, comparse da pochi giorni. Da circa 3 mesi la ragazza presentava acne sul viso che rapidamente si estendeva sul dorso e sul torace, per cui veniva consultato lo specialista dermatologo che prescriveva terapia antibiotica locale senza alcun beneficio. Nel corso del ricovero la paziente iniziava a lamentare dolori articolari in sede lombare che limitavano i movimenti, dolore toracico, che si accentuava con gli atti del respiro, e febbre elevata ad andamento intermittente. Rapidamente compariva anche dolore a livello dell’articolazione tibio-tarsica, che rendeva impossibile la deambulazione. I primi esami di laboratorio evidenziavano leucocitosi neutrofila e aumento degli indici di flogosi (VES, PCR, PCT, alfa proteine); veniva pertanto intrapresa terapia antibiotica sistemica e anti-infiammatoria, con lieve miglioramento della sintomatologia dolorosa.Ai successivi controlli si osservava riduzione della leucocitosi neutrofila e degli indici di flogosi, le sottopopolazioni linfocitarie mostravano aumento dei Linfociti T con un aumentato rapporto CD4/CD8; negativa la ricerca di autoanticorpi e HLA B27. Lo studio radiologico dello scheletro (Rx bacino, femore e mano-polso) evidenziava segni di osteosclerosi. La Scintigrafia Ossea Total Body con Tc 99 confermava un processo osteoblastico attivo, con aree di focale accumulo del tracciante a livello della testa dell’omero destro, del corpo del manubrio sternale e delle clavicole (bull’s head sign), del ginocchio sinistro, dell’articolazione tibio-tarsica sinistra e del piede omolaterale.
La RM permetteva una migliore caratterizzazione delle lesioni ossee evidenziando due lesioni focali della spongiosa (midollar bone lesion), iperintense in T2 a livello di L3 e L4, della testa omerale destra e della clavicola sinistra. Gli elementi clinici e radiologici in nostro possesso, consentivano di porre diagnosi di Sindrome S.A.P.H.O.
Veniva intrapresa terapia medica con Metotrexatei.m. con netta riduzione della sintomatologia dolorosa tanto da permettere la ripresa della deambulazione. Persistendo intenso dolore a livello del rachide lombare e agli arti inferiori, veniva intrapresa terapia con Pamidronatoe.v., associato a Vitamina D e Carbonato di Calcio. L’introduzione del Pamidronato sortiva un netto miglioramento del dolore osteoarticolare che, comunque, non permetteva la sospensione della terapia con FANS; anche le manifestazioni cutanee miglioravano progressivamente. Attualmente la ragazza è in terapia con Metotrexate e Pamidronato, ed esegue stretto follow-up; si valuterà, in seguito, se intraprendere terapia biologica che è stata impiegata con successo in alcuni casi di SAPHO.
Tumori
I tumori toracici e la leucemia raramente si presentano con dolore toracico. Si presume che il dolore sia secondario a compressione meccanica dei nervi intercostali o del midollo allungato, oppure a infiltrazione ossea da parte delle cellule tumorali.
È stato descritto in letteratura il caso di una paziente di 12 anni che presentava da circa 6 mesi un dolore localizzato a livello del torace anteriore e tumefazione sternale. L’anamnesi era negativa per eventi traumatici. L’esame radiografico e la TAC del torace rivelavano una lesione osteolitica che dissolveva la corticale del corpo dello sterno, sia anteriormente che posteriormente, mentre la RMN mostrava un segnale di bassa intensità in T1-pesata e di elevata intensità in T2-pesata. La scintigrafia ossea, eseguita con tecnezio, evidenziava un aumento della captazione del radiofarmaco a livello sternale, del grande trocantere del femore e della estremità della tibia di destra. L’esame radiologico di questi ultimi due distretti ossei, confermava la presenza di lesioni osteolitiche. Sottoposta a biopsia della lesione sternale, la diagnosi istologica fu di “istiocitosi a cellule di Langherans (LCH)”. Venne trattata con chemioterapia (citarabina più vincristina) e la paziente guarì (9).
La localizzazione sternale è estremamente rara, rappresenta infatti, meno dell’1% delle localizzazioni ossee da LCH e, nel79% dei casi, si tratta di lesioni singole. La più frequente sede di localizzazione è il cranio, seguono in ordine decrescente di frequenza: femore, mandibola, pelvi, costole, rachide, scapola, omero e clavicola.
Fumo di sigarette
Il dolore toracico secondario a irritazione polmonare è uno tra i sintomi più comuni dell’esposizione al fumo.
In Italia, sono oltre un milione e duecentomila i giovani fumatori, cioè circa il 20% tra i 15 e i 24 anni con un costante incremento con l’età (10). Recenti dati dimostrano un’età media di inizio del fumo intorno ai 17 anni, senza differenze significative tra maschi (17,2 anni) e femmine (17,8 anni).
Inoltre, solo una minoranza inizia a fumare oltre i 18 anni, mentre 1/5 dei fumatori acquisisce l’abitudine prima dei 15 anni (10), derivandone che per ridurre la diffusione del fumo nei soggetti adulti è indispensabile ridurre il numero delle persone che iniziano a fumare in giovane età mediante interventi molto precoci di prevenzione primaria.
L’esposizione diretta e indiretta al fumo, pone in serio pericolo la salute delle gestanti, dei neonati e dei bambini. I bambini e i neonati esposti al fumo di tabacco, rispetto ai soggetti non esposti, presentano più possibilità di presentare infezioni delle prime vie aeree e asma.
Stupefacenti
Un altro problema emergente è il consumo di sostanze stupefacenti in particolare l’ecstasy, il crack e la cocaina.
Il crack (sotto forma di piccoli cristalli opalescenti) viene da molti preferito alla cocaina in polvere, per i suoi effetti rapidi ed intensi, per il suo basso costo per dose e per la facilità di confezionamento e trasporto della dose. Il crack in granuli, non solubile, si “fuma”. Fumare ha la stessa intensità e rapidità di effetti dell’iniezione endovenosa. Gli abituali consumatori di crack possono presentare una vera epropria sindrome, definita “polmone da crack” (11).
Il dolore toracico, in questi soggetti, è un evento frequente e peggiora nelle profonde inspirazioni. Sembra essere dovuto all’irritazione bronchiale da parte della cocaina stessa, dei prodotti di combustione del crack o dei prodotti utilizzati per favorire la combustione (ad es. butano). Altre cause di dolore toracico che devono comunque essere prese in considerazione nell’utilizzatore di crack sono l’ischemia miocardica acuta, il pneumotorace e il pneumomediastino.
La cocaina può indurre spasmo delle arterie coronarie epicardiche con possibile ischemia e infarto, possibile formazione di trombi endocoronarici da attivazione piastrinica (attraverso l’attivazione della aggregabilità piastrinica indotta dalle catecolamine), proliferazione intimale di cellule muscolari lisce che possono favorire, assieme alla formazione di trombi, l’ostruzione acuta coronarica. La proliferazione intimale potrebbe essere sollecitata da fattori di crescita liberati dalle piastrine. Le modificazioni arteriose intramiocardiche nei cronici consumatori di cocaina, fa si che qualsiasi stimolo che aumenti la domanda di O2 miocardica possa comportare ischemia.
Per quanto esposto, nel sospetto che ci si trovi, dinnanzi a un soggetto che abbia potuto abu- sare di sostanze stupefacenti, deve essere presa in considerazione la possibilità di effettuare uno screening sulle urine e la ricerca dei metaboliti urinari della cocaina.
Meccanismi fisiopatologici responsabilid’ischemia miocardica dopo l’uso di cocaina
La cocaina inibisce la ricaptazione di noradrenalina da parte delle terminazioni nervose adrenergiche e potenzia gli effetti delle catecolamine circolanti sugli organi bersaglio. Ciò provoca un’aumentata stimolazione simpatica del cuore e dei vasi periferici, che determina un maggiore lavoro del cuore e dei vasi periferici, quindi un incremento del consumo di O2. L’aumento del lavoro del cuore in soggetti con coronaropatie può essere il solo meccanismo del dolore toracico da cocaina.
L’aumento delle resistenze nel circolo coronario associato alla tachicardia e all’ipertensione potrebbero spiegare l’ischemia in assenza di coronaropatia.
Caso clinico (osservazione personale)
Un paziente di 21 anni, affetto da microdrepanocitosi, con cattiva compliance alla terapia, dall’età di 16 anni presentava frequenti crisi vasoocclusive che richiedevano l’ospedalizzazionee, mediamente una volta l’anno, si complicavano con broncopolmoniti. Ritenevamo che il peggioramento dell’andamento clinico del paziente fosse da attribuire alla sua usuale cattiva compliance al trattamento. Posto in terapia con idrossiurea il paziente mostrava un netto miglioramento delle condizioni cliniche con scomparsa delle crisi vasoocclusive, sino a quando giungeva al ricovero ospedaliero per astenia ingravescente e dispnea al minimosforzo.
All’EO: condizioni generali scadute, tachicardia, ritmo di galoppo, epatomegalia, qualche rantolo alle basi polmonari. L’esame ecocardiografico rivelava un alterato rilasciamento diastolico del ventricolo destro, ventricolo sinistro di dimensioni conservate con depressa cinesi globale (FE = 46%), ipertensione polmonare, ingrandite le sezioni di destra. Nel sospetto di microembolia polmonare veniva sottoposto a scintigrafia polmonare che mostrava una disomogenea distribuzione parenchimale del radiofarmaco nel terzo medio superiore del polmone destro, con area più decisamente fredda in sede apicale, nel terzo medioanteriore e più piccola in sede mantellare. Posto in trattamento specifico si assisteva a un miglioramento delle condizioni cliniche che ne permettevano la dimissione.
A 6 mesi di distanza si rendeva necessario un nuovo ricovero a causa del ripresentarsi della sintomatologia caratterizzata da astenia intensa e dispnea al minimo sforzo. ECG: tachicardia bsinusale, extrasistolia ventricolare trigemina. Ecocardiografia: funzione sistolica non valutabile. Scintigrafia polmonare: irregolare e disomogenea la distribuzione del radiofarmaco con presenza di multiple aree fredde in entrambi i polmoni, soprattutto a destra.
Indagando sulle abitudini di vita del ragazzo, si apprendeva che sin dall’epoca del primo ricovero aveva iniziato far uso di sostanze stupefacenti, fumando cocaina e crack, con probabile effetto di vasocostrizione della circolazione polmonare, proliferazione delle cellule muscolari lisce della media e dell’intima dei vasi, maggiore consumo d’ossigeno. Tutto ciò predisponeva il paziente alle crisi vaso-occlusive, nonostante il trattamento della patologia di base.
Effetti del consumo di marijuana
L’uso della cannabis produce effetti tossici a livello dell’apparato respiratorio per esposizione sia di breve che di lunga durata: frequenza di assunzione e quantità assunte rappresentano un fattore fondamentale nel determinismo di eventuali patologie polmonari.
Va tenuto presente che i soggetti che abusano di cannabis sono in elevata percentuale (69%) anche fumatori di tabacco ed è quindi difficile distinguere gli effetti del fumo di cannabis rispetto a quelli ampiamente noti del tabacco (12). Sebbene studi clinici di questo tipo siano rari e non tutti concordi, la maggioranza delle ricerche dimostra come l’effetto della cannabis esplichi un effetto additivo nei confronti del tabagismo. La particolare modalità di aspirazione dello “spinello” (inspirazione profonda e prolungata seguita da una manovra di Valsalva) espone il polmone ad un contatto quantitativamente maggiore e prolungato con le sostanze in esso contenute, rispetto ad una sigaretta di tabacco; è infatti dimostrato che i livelli di monossido di carbonio e di deposito di catrame sono rispettivamente cinque e quattro volte superiori dopo assunzione di uno spinello rispetto ad una singola sigaretta.
In uno studio longitudinale è stato evidenziato come il piccolo ma significativo decremento del volume medio espiratorio forzato al primo secondo (FEV1) negli utilizzatori di cannabis è il doppio di quello attribuibile al fumo di tabacco. Anche dopo robuste ma brevi esposizioni al fumo di cannabis (5 spinelli al giorno per 6-8 settimane) si sviluppano significative riduzioni, dose dipendenti, della FEV, reversibile dopo cessazione dell’uso. La presenza di tosse, catarro, dispnea, sibili sono risultati essere più frequenti negli abituali consumatori rispetto ai non consumatori.
Le principali conseguenze che possono derivare dall’uso della cannabis sono: cronica infiammazione delle vie aeree, granulomi, pneumotorace, tumori e infezioni (contaminazione della cannabis da parte di batteri gram negativi e/o spore fungine), danno del tappeto muco ciliare o cambiamenti nella competenza immunologica locale.
Avvelenamento da monossido di carbonio (CO)
L’avvelenamento da monossido di carbonio è la più frequente causa di morte da avvelenamento accidentale in ogni età, ma sovente non viene riconosciuto tempestivamente per l’aspecificità dei sintomi. Non a caso il monossido di carbonio viene soprannominato il “killer silenzioso”: è un veleno allo stato gassoso, incolore, insapore inodore; questo viene prodotto dalla incompleta combustione, per carenza di ossigeno (la combustione completa porta alla formazione di anidride carbonica) di legna, carbone, petrolio, kerosene, metano, propano.
Nell’ambiente domestico sono presenti numerose possibili fonti di avvelenamento, come im- pianti di riscaldamento autonomo con cattiva manutenzione e ambienti inadeguati, grill a car- bone, camini o focolari difettosi, asciugatori per vestiti, fuochi, fumo da sigaretta, etc.
La sintomatologia spesso è subdola; poiché si verifica maggiormente nel periodo invernale viene spesso scambiata per una banale virosi delle vie aeree. Il CO determina ipossia tissutale attraverso due meccanismi: si lega all’Hb nello stesso sito dell’ossigeno formando la carbossiemoglobina (COHb) che, a causa della sua affinità per l’Hb> di 250 volte rispetto a quello dell’O2, provoca un grave blocco del trasporto dell’O2; provoca uno spostamento a sinistra della curva di dissociazione dell’ossiemoglobina residua, riducendone pertanto la capacità di cedere O2 ai tessuti. Un ulteriore danno tissutale può essere provocato dal legame del CO con altre proteine della cellula (enzimi della respirazione cellulare). La quantità di monossido di carbonio assorbita è direttamente proporzionale alla durata dell’esposizione, alla concentrazione nell’ambiente e alla ventilazione stessa. Difficilmente si pensa che il dolore toracico, accompagnato da tachicardia, possa essere un sintomo da riferire ad avvelenamento da CO. I casi di pazienti che hanno presentato un interessamento cardiaco, con quadri che vanno dall’aritmia all’infarto miocardico, vengono per lo più descritti in persone con pregressa cardiopatia, anche se oggi appaiono segnalazioni simili in età pediatrica e adolescenziale. Nel sospetto di avvelenamento da monossido di carbonio è indispensabile eseguire la determinazione della COHb (valori normali 1-3%; nei fumatori 5-6%). Per meglio definire la gravità dell’avvelenamento da CO, le indagini da eseguire comprenderanno anche i biomarcatori cardiaci, la cui elevazione si associa a necrosi cardiaca e muscolare (troponina cardiaca, mioglobina, CPK-MB, peptide natriuretico tipo B). Il trattamento comprende l’allontanamento dall’ambiente in cui è avvenuta l’esposizione al monossido di carbonio, somministrazione di ossigeno al 100% (da mantenere sino alla normalizzazione dei valori della COHb). L’emivita della COHb è di 4-6 ore in aria ambiente, di 1 ora respirando ossigeno puro e si riduce a 15-30 minuti in camera iperbarica. Bambini e adolescenti con sintomi aspecifici quali cefalea e/o vertigini, polipnea, dolore toracico e tachicardia potrebbero essere vittime di avvelenamento da monossido di carbonio. Inoltre, dolore toracico e tachicardia con obiettività clinica negativa dovrebbero venir riconosciuti come espressione d’ipossia. Nel sospetto di esposizione al CO, il paziente, insieme al suo nucleo familiare, dovrebbe essere sottoposto a screening per dosaggio della COHb, onde evitare pericolose sottovalutazioni con conseguenze, purtroppo, non infrequentemente tragiche.
Cause Cardiache
Il dolore toracico di natura cardiogena è un evento raro in età pediatrica e adolescenziale, con una prevalenza inferiore al 6%(30). Nella Tabella 2, vengono riportate le più comuni cause cardiache di dolore toracico in età pediatrico-adolescenziale (2).
Cause Psicogene
I disturbi psicogeni rappresentano dal 5-10% delle cause di dolore toracico nei bambini. L’incidenza è più elevata durante l’adolescenza e nel sesso femminile. È possibile ipotizzare un disturbo psicogeno in presenza di ansia ed eventi stressanti (morti per malattie cardiovascolari o malattie in familiari, separazione o divorzio dei genitori, abuso fisico o sessuale, attacchi di panico); si osserva una netta discrepanza tra la severità dei disturbi che il soggetto accusa e il reperto obiettivo assolutamente negativo(2). Il dolore toracico, non infrequentemente, si associa a dolori addominali ricorrenti e cefalea.
Conclusioni
Una buona conoscenza della fisiopatologia e dell’anatomia del torace contribuirà a finalizzare l’esame obiettivo ed il percorsodiagnostico-terapeutico dell’adolescente con dolore toracico (Tabella 3).
Le alterazioni della parete toracica rientrano tra le cause più comuni delle toracoalgie e sono, generalmente, facilmente riproducibili. In questi casi vi è un’irritazione dei tessuti parietali dai- quali partono gli stimoli che, seguendo i nervi intercostali, raggiungono i gangli delle radici dorsali, percorrono le vie spinali afferenti e arrivano ai centri cerebrali, dove sono interpretati come dolori netti, superficiali e localizzati. È possibile, inoltre, che uno stimolo doloroso, nato da un’irritazione primitiva di una radice dorsale, sia riferito alla parete toracica, come si verifica nel caso delle radicoliti. Le strutture somatiche e viscerali hanno alcune vie nervose sensoriali in comune e, pertanto, un disturbo viscerale può esprimersi con manifestazioni dolorose a livello T1-T6.
Anche i problemi addominali possono causare dolore toracico in quanto le porzioni posteriori e laterali del diaframma sono innervate dai nervi intercostali e possono, pertanto, “riferire” la sensazione dolorosa al torace inferiore e all’addome; il sistema d’innervazione della porzione centrale e di quella anteriore, invece, determina un fenomeno di sinalgia delle regioni della spalla e del collo.
Nel corso dell’esame obiettivo dovranno essere valutati i segni vitali e si dovrà effettuare un’attenta valutazione (percussione e palpazione)delle pareti toraciche e dell’addome e dell’apparato cardiaco e respiratorio (auscultazione). Dovranno essere sempre esclusi possibili traumi toracici. Per quanto concerne l’impiego di esami strumentali, la valutazione dovrà comprendere una radiografia del torace. Ulteriori esami (di laboratorio e/o strumentali) quali emogasanalisi, enzimi miocardiaci, ECG (a riposo, dopo sforzo, Holter), ecocardiografia, scintigrafia polmonare, ecografia addominale, sono raramente necessari a meno che non vi siano indicazioni specifiche raccolte dall’anamnesi e/o dall’esame obiettivo.
Il paziente che giunge alla nostra osservazione sintomatico, con un dolore non palesemente di natura funzionale o muscolo scheletrico, dovrà essere sottoposto ad ossigenoterapia e monitoraggio cardio-respiraraOverride-9″>L’approccio al dolore toracico nell’adolescente dovrà essere affrontato tenendo conto sia degli aspetti somatici che di quelli psicosociali, data la loro stretta connessione e reciproca influenza.
Il corretto approccio clinico e metodologico, eviterà inutili, stressanti e costose indagini.
Tabelle
Tabella I. Prevalenza del dolore toracico in età pediatrico adolescenziale
|
Dolore toracico idiopatico |
12-85% |
|||
|
Muscoloscheletrico • Costocondrite/sindrome costosternale • Sindrome di Tietze • Sindrome da scivolamento costale • Traumi o stiramento dei muscoli • Xifodinia • Malformazioni vertebrali |
15-31% |
Miscellanea • Drepanocitosi • Cause mammarie • Malattia di Bornholm Sindrome S.A.P.H.O. • Herpes Zoster • Compressione nervosa • Droghe • Fumo da sigarette |
4-21% |
|
|
Polmonare • Asma • Asma da sforzo • Bronchite • Pleurite • Polmonite • Pneumotorace • Embolia polmonare • Sindrome toracica acuta |
12-21% |
Cardiaco |
6% |
|
|
Psicogeno |
5-17% |
|||
|
Gastrointestinale • Reflusso gastro-esofageo • Spasmo esofageo • Esofagite/gastrite iatrogena • Ernia iatale • Ulcera peptica • Colecistite |
8% |
|||
Tabella II. Cause cardiache di dolore toracico
|
Infiammatorie: pericarditi, miocarditi (infettive: virus, batteri; non infettive: LES, M. di Crohn, sindrome post cardiotomica |
|
Aumentata richiesta miocardica di ossigeno o ridotta disponibilità: cardiomiopatia (dilatativa o iper- trofica), stenosi aortica, stenosi subaortica, stenosi aortica sopravalvolare, aritmie |
|
Anomalie delle arterie coronarie: congenite e acquisite (arterite coronaria-malattia di Kawasaki, post chirurgiche, vasculopatia coronarica post trapianto, ipercolesterolemia familiare, diabete mellito) |
|
Miscellanea: dissecazione aortica, rottura di aneurisma aortico, ipertensione polmonare, mixomi atriali, device cardiaci/stent |
|
Droghe: cocaina, overdose di sostanze simpaticomimetiche |
Tabella III. Dolore toracico nell’adolescenza: strategia d’intervento in base alla sintomatologia
|
Sintomi |
Tipo d’intervento |
|
Dolore toracico acuto presumibilmente funzionale o idiopatico |
Follow-up e indagini specifiche in base alla sintomatologia clinica |
|
Dolore toracico associato a palpitazioni, sincope o patologia cardiaca sottostante |
Valutazione cardiologica ed eventuali esami strumentali (ECG, ecocardiografia, ecc.) |
|
Dolore toracico secondario a una causa specifica sottostante |
Ulteriori approfondimenti sulla base della valutazione clinica |
|
Dolore toracico cronico funzionale o idiopatico |
Approfondimento diagnostico per sospetta origine psichiatrica, asma o patologia gastroesofagea |
Bibliografia
1. Raiola G, Galati MC, De Sanctis V, et al. Il dolore toracico nell’adolescente. Minerva Pediatr 2002; 54:623-630.
2. Surendranath Ret al. Chest Pain in Children and Adolescents. Pediatrics in Review 2010;Vol. 31(1): e1-e9
3. Risch WD et al. The effect of graded immersion on heart volume, central venous pressure, pulmonary blood distribution, and heart rate in man. Pflugers Arch 1978; 374:115-118.
4. Uchida K et al. Acute aortic dissection occurring during butterfly stroke in a 12-year-old boy. Interact CardiovascThoracSurg 2009; 9:366-368.
5. Buck JR et al. Pulmonary embolism in children. ] PediatrSurg 1981; 16:385 391.
6. Evangelista J et al. Chest pain in children: diagnosis through history and physical examination. J Pediatr HealthCare 2000; 14:3.
7. BK Kunduet al. “Diagnosing the SAPHO syndrome: a report of three cases and review of literature” ClinRheumatol (2013) 32: 1237-1243
8. M Raviero-Barciela et al. Palmoplantarpustolosis and chest pain. Lancet, 2012; 5; 379 (9827).
9. Tsuchie Het al. Langerhans cell histiocytosisof the sternum. Ups J Med Sci. 2009; 114:121-125.
10. Pacifici R. Tabagismo e Servizio Sanitario Nazionale: prospettive ed impegni. X Convegno Nazionale: Tabagismo e Servizio Sanitario Nazionale, 30 maggio 2008; www.iss.it
11. Haim DY et al. The pulmonary complications of crack cocaine. A comprensive review. Chest 1995;107:233-240.
12. Poulton RG et al. Prevalence and correlates of cannabis use and dependence in young New Zealanders. NZ Med J 1997; 110:68-70.